
| A. | 1:36 | B. | 2:35 | C. | 5:32 | D. | 4:33 |
分析 根据充分反应后生成36g水,利用化学反应方程式可知,4g氢气和32g氧气恰好完全反应生成36g水,则37g混合气体有剩余的气体存在,则有两种可能:①剩余气体为氢气;②剩余气体为氧气来分析解答.
解答 解:设参加反应反应的氢气和氧气的质量分别为x,y;
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
4 32 36
x y 36g
$\frac{4}{x}=\frac{32}{y}=\frac{36}{36g}$
x=4g
y=32g
①若剩余气体为氢气,则氢气的质量为4g+(37g-36g)=5g,即混合气体中有5g氢气和32g氧气;则氢气和氧气的质量比5:32;
②若剩余气体为氧气,则氧气的质量为32g+(37g-36g)=33g,即混合气体中有4g氢气和33g氧气,则氢气和氧气的质量比为4:33.
故选CD.
点评 本题考查学生利用化学反应方程式的计算来分析混合物的成分,学生应能利用化学反应判断恰好完全反应的量,要注意过量计算过程的思维训练.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
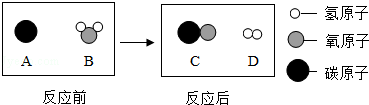
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
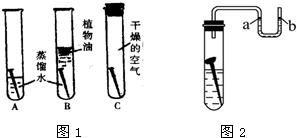
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaCl | B. | C1O2 | C. | Cl2 | D. | HC1O3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.
人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com