
| 二氧化锰 |


科目:初中化学 来源: 题型:
| A、用100mL量筒量取8.5mL水 |
| B、用托盘天平称得某食盐样品为15.6g |
| C、用烧杯量取180.0mL稀盐酸 |
| D、测得室内空气中氧气所占体积分数为19% |
查看答案和解析>>
科目:初中化学 来源: 题型:

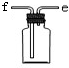
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤及操作 | 实验现象 | 结论 |
| ①在蒸馏水中加入少量的明矾,搅拌静置 | 明矾全部溶解 | 明矾能溶于水 |
| ②在浑浊的井水中加入少量的明矾,搅拌静置 | 井水变澄清 | 明矾能净水 |
| ③在浑浊的井水中加入少量的Al2(SO4)3,搅拌静置 | 井水变澄清 | Al2(SO4)3能净水 |
| ④在浑浊的井水中加入少量的K2SO4,搅拌静置 | 井水仍浑浊 | (1) |
| ⑤在浑浊的井水中加入少量的KCl,搅拌静置 | 井水仍浑浊 | (2) |
| ⑥在浑浊的井水中加入少量的AlCl3,搅拌静置 | 井水变澄清 | (3) |
| 由以上实验可知:明矾的净水作用与Al3+ 有很大的关系. | ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com