
| 高铁酸钾的质量 |
| 样品的质量 |
| ||
| 792 |
| x |
| 96 |
| 0.672L×1.429g/L |
| 7.92g |
| 10g |


科目:初中化学 来源: 题型:
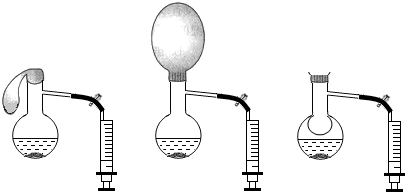 在蒸馏烧瓶内加适量固体X和液体Y,观察气球逐渐胀大.打开弹簧夹,将注射器中液体Z注入烧瓶并振荡,气球缩小并被吸入烧瓶内.则X、Y、Z分别是( )
在蒸馏烧瓶内加适量固体X和液体Y,观察气球逐渐胀大.打开弹簧夹,将注射器中液体Z注入烧瓶并振荡,气球缩小并被吸入烧瓶内.则X、Y、Z分别是( )| X | Y | Z | |
| A | Zn | 稀盐酸 | 石灰水 |
| B | CaO | 水 | 稀盐酸 |
| C | Na2CO3 | 稀硫酸 | NaOH溶液 |
| D | NaOH | 水 | 稀硫酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、中和反应前后溶液中水的质量相等 |
| B、饱和溶液降温浓度可能不变 |
| C、某溶液继续加入另一种溶质,原溶质浓度会变大 |
| D、溶液不一定是混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com