
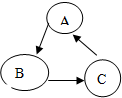
 已知A、B、C是初中化学常见的物质,其转化关系如图所示:若A、B、C均含有同一种金属元素,A为红色的金属单质,B是A的氧化物,C为蓝色液体,则:(填化学式)A为Cu,写出一个符合C→A转化关系的化学方程式是:Fe+CuSO4═FeSO4+Cu.此方程的反应类型属于置换反应.
已知A、B、C是初中化学常见的物质,其转化关系如图所示:若A、B、C均含有同一种金属元素,A为红色的金属单质,B是A的氧化物,C为蓝色液体,则:(填化学式)A为Cu,写出一个符合C→A转化关系的化学方程式是:Fe+CuSO4═FeSO4+Cu.此方程的反应类型属于置换反应.  激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:初中化学 来源: 题型:实验探究题
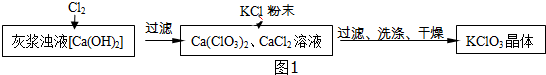
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
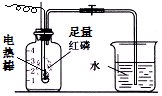 按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图所示用带火星的木条分别以甲、乙两种方式迅速插入盛满氧气的集气瓶中,观察到木条复燃,且在甲中燃烧比乙中燃烧更旺.上述实验说明氧气具有的性质是:
如图所示用带火星的木条分别以甲、乙两种方式迅速插入盛满氧气的集气瓶中,观察到木条复燃,且在甲中燃烧比乙中燃烧更旺.上述实验说明氧气具有的性质是:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含钾的化合物 | B. | 含钠的化合物 | C. | 含钙的化合物 | D. | 含铁的化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图为某品牌牛奶的部分标签,请据此回答下列问题[第(2)-(3)题用标签中的序号填写]:
如图为某品牌牛奶的部分标签,请据此回答下列问题[第(2)-(3)题用标签中的序号填写]:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com