
分析 (1)根据过滤的原理分析判断;
(2)根据溶液的酸碱性与酸碱度的关系分析;
(3)带有酸臭味的城市生活污水显酸性;
(4)根据防止水污染的措施分析判断.
解答 解:(1)难溶物不溶于水,故用过滤法除去;故填:②.
(2)pH大于7,则说明该水样显碱性.故填:碱.
(3)带有酸臭味的城市生活污水显酸性,化工厂排放的污水可能显碱性.故填:②.
(4)①抑制水中所有动、植物的生长,是不现实的;
②不任意排放工业废水,能防止水的污染;
③禁止使用农药和化肥,是不现实的,农业的发展离不开农药和化肥;
④生活污水经过净化处理后再排放,能防止水的污染;
故选②④.
点评 本题主要考查净化水的方法和节约用水的重要性,要树立节约用水人人有责的理念.


科目:初中化学 来源: 题型:选择题
| A. | 就地焚烧以处理城市生活垃圾 | |
| B. | 使用脱硫煤可以减少酸雨 | |
| C. | 禁止使用化肥以减少水体污染 | |
| D. | 提倡使用一次性筷子以减少洗涤环节 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 步骤③的现象 | 步骤⑥的结果 | 步骤⑦的现象 | 结论 |
| 带火星的木条复燃 | 0.2g | 带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
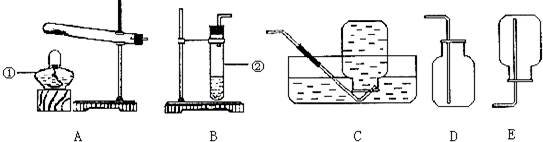
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 冰水、四氧化三铁、铁 | B. | 澄清的石灰水、自来水、液态氮 | ||
| C. | 洁净的空气、冰、水银 | D. | 加碘食盐、氯酸钾、红磷 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 早在春秋战国时期,我国就开始生产和使用铁器,从1世纪起,铁便成了一种最主要的金属材料.2010年中国粗钢产量已超过6亿吨.如图是工业上炼铁的高炉,制造炼铁高炉的金属材料需要具备的物理性质是(1)熔点高、耐高温(写一条即可),焦炭燃烧生成还原剂CO的过程中的能量转化是化学能转化为热能和光能,该变化是石灰石的主要成分分解产物中的金属氧化物和炉渣中的某种成分发生反应,生成硅酸钙(CaSiO3)的过程中,用化学方程式表示为CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3,变化前后硅元素的化合价分别为+4、+4.
早在春秋战国时期,我国就开始生产和使用铁器,从1世纪起,铁便成了一种最主要的金属材料.2010年中国粗钢产量已超过6亿吨.如图是工业上炼铁的高炉,制造炼铁高炉的金属材料需要具备的物理性质是(1)熔点高、耐高温(写一条即可),焦炭燃烧生成还原剂CO的过程中的能量转化是化学能转化为热能和光能,该变化是石灰石的主要成分分解产物中的金属氧化物和炉渣中的某种成分发生反应,生成硅酸钙(CaSiO3)的过程中,用化学方程式表示为CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3,变化前后硅元素的化合价分别为+4、+4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com