
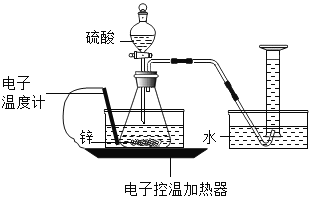
【题目】某实验小组的同学对“锌与硫酸反应速率的影响因素”进行探究,并利用如图装置收集产生的氢气。
(查阅资料)
圆粒状锌的直径通常为 3-4 毫米,粉末状锌的直径通常为 0.3-0.5 毫米。
(进行实验)
实验 1:在不同温度下,进行锌与硫酸反应的实验。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
1-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
1-2 | 30 | 20 | 10% | 圆粒状 | 1 | 134 |
1-3 | 40 | 20 | 10% | 圆粒状 | 1 | 107 |
实验 2:在相同温度下,继续进行锌与硫酸反应速率的影响因素的探究。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
2-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
2-2 | 20 | 20 | 10% | 粉末状 | 1 | 47 |
2-3 | 20 | 20 | 20% | 圆粒状 | 1 | 88 |
2-4 | 20 | 20 | 20% | 粉末状 | 1 | 26 |
(解释与结论)
(1)锌与硫酸反应的化学方程式为_____ 。
(2)能用排水法收集氢气的原因是氢气_____(填“易”或“难”)溶于水。
(3)实验 1 的目的是_____。
(4)实验 2 中,欲得出“其他条件相同时,硫酸的溶质质量分数越大,锌与硫酸反应的速率越快”的结论,需要对比的实验_____(填编号)。
(5)实验 2 中,通过对比 2-1 和 2-2,得出的结论是_____。
(反思与评价)
(6)实验室制取氢气时,通常使用锌粒而不用锌粉的原因为_____。
(7)实验室中若使用 6.5g 锌粒制取氢气,理论上制得氢气的质量为_____g。
【答案】Zn+ H2SO4 =ZnSO4 + H2↑ 难 探究温度对锌与硫酸反应速率的影响 2-1与2-3(或2-2与2-4) 其他条件相同时,锌与硫酸接触面积越大反应速率越快 使用锌粉反应速率过快,不利于控制反应 0.2
【解析】
[解释与结论]
(1)锌与硫酸反应生成硫酸锌和氢气,化学方程式为Zn+ H2SO4 =ZnSO4 + H2↑;
(2)能用排水法收集氢气的原因是氢气难溶于水;
(3)实验1中 ,形成对照的实验间,只有温度不同,其他影响反应速率的因素都相同,故目的是探究温度对锌与硫酸反应速率的影响;
(4)实验 2 中,欲得出“其他条件相同时,硫酸的溶质质量分数越大,锌与硫酸反应的速率越快”的结论,需要对比的实验是只有硫酸浓度不同,其他都相同的实验2-1与2-3(或2-2与2-4);
(5)实验 2 中,对比2-1和 2-2中,只有锌粒的形状不同,即锌与酸的接触面积不同,且颗粒越小,锌与酸的接触面积越大,反应越快,得出的结论是其他条件相同时,锌与硫酸接触面积越大反应速率越快;
[反思与评价]
(6)实验室制取氢气时,通常使用锌粒而不用锌粉的原因为使用锌粉反应速率过快,不利于控制反应;
(7)实验室中若使用 6.5g 锌粒制取氢气,设理论上制得氢气的质量为x,则: ![]()
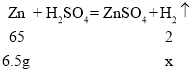
![]() x=0.2g
x=0.2g


科目:初中化学 来源: 题型:
【题目】请用你具备的化学知识回答下面问题:
(1)收集二氧化碳不能用排水法原因是_____________________。
(2)夏天铁轨之间的缝隙变小的微观原因是_____________________。
(3)“洁厕灵”与“漂白精”不能混用,两者若混合易产生一种有毒气体X。 反应原理为:![]() ,则X的化学式为_____________________。
,则X的化学式为_____________________。
(4)暖气片表面常刷“银粉”(主要成分是铝)利用的是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
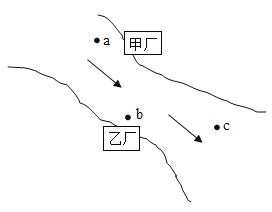
【题目】甲、乙两化工厂分布在某排污渠两岸(如图所示),箭头代表水流方向。若甲厂附近a处水样经检测含有的阴离子是OH-、SO42- ,c处水样经检测pH=7且只含有少量的NaCl,则乙厂排放到b处水中的物质可能是( )
A.BaCl2、HC1
B.H2SO4、Ba(NO3)2
C.MgSO4、NaCl
D.BaCl2、Mg(NO3)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】农业上常用质量分数为16%的NaCl溶液选种。实验室配制100 g该浓度溶液的过程如下图所示。下列说法不正确的是

A. 实验操作顺序为④②①⑤③B. ②中需称量NaCl的质量为16 g
C. 选用100 mL量筒量取所需水的体积D. ①中有部分固体洒落所得溶液的浓度偏大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组做了如下图所示实验。
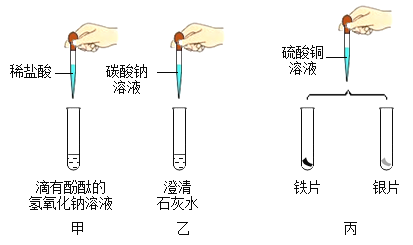
(1)能证明甲中发生反应的现象是_____。
(2)乙中可观察到的现象是_____,发生反应的化学方程式为_____。
(3)丙中观察到的现象为_____, 由该实验现象推断,三种金属活动性由强到弱为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是氢氧化钠溶液与稀盐酸反应的微观示意图,请回答下列问题:
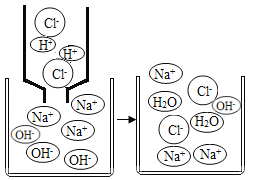
(1)酸和碱反应生成_____和水叫中和反应。
(2)反应后该溶液的pH_____7(填“>”、“<”或“=”),往溶液中滴加数滴酚酞试液,溶液_____。
(3)写出该反应的方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氨基钠(NaNH2)常用于医药制造,根据其性质,氨基钠应该用时制备,不要长时间贮存。工业上制取氨基钠是将钠于97~100℃熔融,向反应容器中缓慢通入无水液氨(NH3),再加热至350~360℃,生成氨基钠和氢气。下列说法中,不正确的是( )
A. 氨基钠的化学性质稳定
B. 将钠于97~100℃熔融属于物理变化
C. 制取氨基钠的反应方程式为:2Na + 2NH3 ![]() 2NaNH2+H2↑
2NaNH2+H2↑
D. 通入无水液氨的原因是,钠可能与水反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室利用如图所示装置进行相关实验。
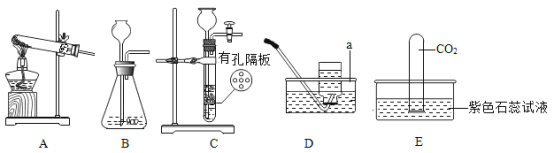
(1)装置D中仪器a的名称是_____。
(2)用一定量氯酸钾和二氧化锰混合加热制取氧气时。
Ⅰ.反应的化学方程式为_____,反应类型是_____ (填“化合”或“分解”)反应。
Ⅱ.下图是用D装置收集氧气的过程,依次观察到的现象是_____ (用字母表示)
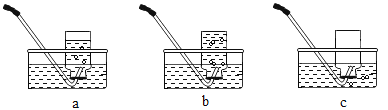
Ⅲ.实验结束后,经过溶解、_____、 洗涤、 烘干等操作回收二氧化锰。
Ⅳ. 反应过程中,能正确表示对应变化关系的图像是_____(填字母编号)。
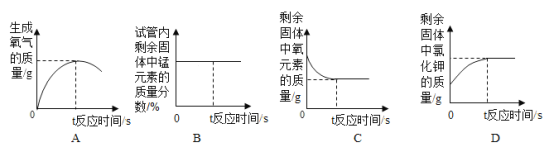
(3)用块状大理石和稀盐酸制取二氧化碳时。
Ⅰ.可选用发生装置B或_____(填编号);在装置B中依次添加大理石、盐酸,添加盐酸时从长颈漏斗中倒入锥形瓶至_____。
Ⅱ.将收集满二氧化碳气体的试管倒插入紫色石蕊试液中(见上图E装置),并轻轻振荡试管。产生的现象是_____; 反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
物质 | A | B | C | D |
反应前质量 |
|
|
|
|
反应后质量 | 待测 |
| 0 |
|
下列说法正确的是![]()
A. 物质C一定是反应物,物质D可能是单质
B. 反应后密闭容器中A的质量为![]()
C. 反应过程中,物质B和物质D变化的质量比为87:36
D. 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com