
| ��1�� | ��2�� | ��3�� | |
| h1/���� | 11.0 | 11.4 | 11.6 |
| h2/���� | 8.7 | 9.1 | 9.2 |
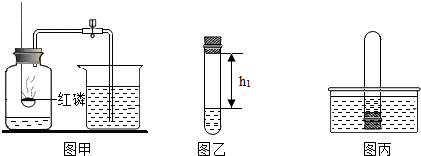
���� ��1��������Ϣ�����ƺ�������ˮ��Ӧ��������������ƣ����ʵ��Ŀ�ķ�����ԭ��
��2������h1��h2�ĸ߶Ȳ��֪����������������������������ļ���ó������
��3���������ֱ���ķ���ʹ�õ�ԭ�����жԱȷ�����
��� �⣺��1�������Ƶ�������������������˳����Ŀ����ʹ��������ַ�Ӧ��ʹ�����ȷ��
��2��h1��h2�ĸ߶Ȳ�����������������������������������=$\frac{���������}{���������}$��100%=$\frac{11.0-8.7}{11.0}$��100%=20.9%�����20.9%��
��3��С����Ƶ�ʵ�������������������������������µ����壬����������ٵ������������������Ӷ���������������������α�������������Ҳ�������µ����壬������ѹ��ˮѹ��װ���ڣ�����������������������ԭ�����ƣ������ֻ���Ŀ����е������Ҳ������µ����壨�������ɣ�
�𰸣�
��1��ʹ��Ӧ���ַ�Ӧ��
��2��20.9%��
��3�����ܡ�װ�ü������Ժõȣ�
���� ����ͨ����Ϣ����ʽ��Ҫ�����òⶨ����������������ʵ��ԭ�����������衢ʵ����۵ȣ�������ѧ���ķ�������������֪ʶǨ������������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������� | B�� | ���ϲ��� | C�� | �л��ϳɲ��� | D�� | ���ǽ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȣ��棩 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| SiO2 | AI2O3 | Fe2O3 | CaO | MgO | K2O | Na2O |
| 69.15% | 17.94% | 0.48% | 0.09% | 0.16% | 9.75% | 1.90% |
| A�� | ������ | B�� | ���� | C�� | ����� | D�� | ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���������з������ó��ٽ������̼��Ϊ����Ⱦɫ����ˮȾɫ�����������ӡȾ��֯��ҵ���ٵĻ�����Ⱦ���⣬���ٽ������̼�Ƕ�����̼���¶Ⱥ�ѹǿ�����ٽ��ʱ�����������ʵ�����״̬�����ʣ������йس��ٽ������̼��ȷ���ǣ�������
���������з������ó��ٽ������̼��Ϊ����Ⱦɫ����ˮȾɫ�����������ӡȾ��֯��ҵ���ٵĻ�����Ⱦ���⣬���ٽ������̼�Ƕ�����̼���¶Ⱥ�ѹǿ�����ٽ��ʱ�����������ʵ�����״̬�����ʣ������йس��ٽ������̼��ȷ���ǣ�������| A�� | ���ٽ�CO2������һ����������ʣ�����ȼ�� | |
| B�� | ���ٽ�CO2������һ����ɱ���ѧ��ɲ�ͬ������ | |
| C�� | ���ٽ�CO2����ɴ��������к����ж�����ȼ���ܼ� | |
| D�� | ���ٽ������̼������̬��Һ̬֮���ת���ǻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com