
分析 (1)根据已有的铁的冶炼和生锈的知识进行分析解答,一氧化碳能与氧化铁反应生成铁和二氧化碳;
(2)考虑铝在常温下能跟氧气发生反应,生成一种致密而坚固的氧化铝薄膜;
(3)根据镁的金属活动性比铜、铁强,镁会先于氯化铜反应,置换出铜进行分析;
(4)根据金属与酸、盐的溶液反应的规律书写化学方程式.
解答 解:
(1)一氧化碳与氧化铁高温反应生成铁和二氧化碳,故其化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)铝制品不易生锈而铁制品容易生锈,是因为铝在常温下能跟氧气发生反应,生成一种致密而坚固的氧化铝薄膜,阻止了内层的铝进一步被氧化,从而对铝制品起到保护作用;
(3)镁的金属活动性比铜、铁强,镁会先于氯化铜反应,置换出铜,所以在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液.①滤液中一定含有的溶质是MgCl2;②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是Cu、Fe.故填:MgCl2;Cu、Fe;
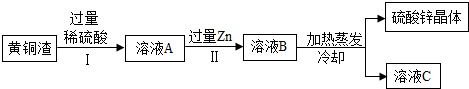
(4))①由于锌排在氢和铜的前面,故锌既可以与酸反应,也可以与硫酸铜反应,反应的化学方程式分别为H2SO4+Zn═ZnSO4+H2↑;CuSO4+Zn═ZnSO4+Cu.
②A、由图可知,操作Ⅰ过滤除去铜和杂质,操作Ⅱ过滤是除去锌和置换出的铜;
B、因氧化锌的质量大于氧化铜,另外锌也能和硫酸反应生成硫酸锌,而铜和硫酸不反应,故溶液A中硫酸锌的质量大于硫酸铜;
C、溶液A加入锌后,反应的化学方程式分别为:H2SO4+Zn═ZnSO4+H2↑;CuSO4+Zn═ZnSO4+Cu;对反应H2SO4+Zn═ZnSO4+H2↑分析可知,每65份质量的锌进入溶液,从溶液中出来2份质量的氢气,使得溶液质量增加,对于反应CuSO4+Zn═ZnSO4+Cu来说,每65份质量的锌进入溶液,从溶液中析出64份质量的铜,也使得溶液质量增大;故溶液A的质量小于溶液B;
D、溶液C为饱和溶液,质量分数达到同温度下的最大值,故D错误;
故选D.
故答案为:
(1)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)铝在常温下能跟氧气发生反应,生成一种致密而坚固的氧化铝薄膜,阻止了内层的铝进一步被氧化,从而对铝制品起到保护作用;
(3)①MgCl2; ②Cu、Fe;(4)①Zn+H2SO4=ZnSO4+H2↑; ②D.
点评 本题考查的是金属与金属材料的知识,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 硝酸银溶液见光易分解,因此需要保存在棕色的试剂瓶中,为测定实验室中一瓶久置的AgNO3溶液中溶质的质量分数,取50g该溶液,并向其中加入NaCl溶液,测定结果如图所示.
硝酸银溶液见光易分解,因此需要保存在棕色的试剂瓶中,为测定实验室中一瓶久置的AgNO3溶液中溶质的质量分数,取50g该溶液,并向其中加入NaCl溶液,测定结果如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用熟石灰改良酸性土壤 | |
| B. | 用氢氧化钠溶液洗涤石油产品中的残留硫酸 | |
| C. | 用浓硫酸干燥湿润的氧气 | |
| D. | 服用含氢氧化铝的药物治疗胃酸过多 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 15g碳酸钙和15g碳酸钠 | B. | 1.8g铝粉和1.8g铁粉 | ||
| C. | 4.2g碳酸氢钠和4.2g碳酸镁 | D. | 2.2g氧化铜粉末和2.4g镁条 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
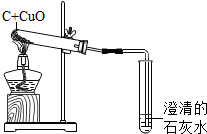 如图是碳和氧化铜在-定条件下进行反应的实验装置,该反应需几分钟时间.
如图是碳和氧化铜在-定条件下进行反应的实验装置,该反应需几分钟时间.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
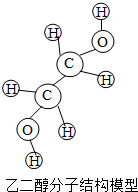 乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.
乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.| A. | 乙二醇的化学式为C2H602 | |
| B. | 乙二醇是由碳、氢、氧三种原子构成的 | |
| C. | 乙二醇与水不能形成饱和溶液 | |
| D. | 乙二醇可以用作汽车的防冻剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
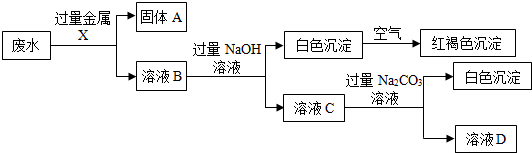
| A. | 在①中,向一份滤液中加入过量NaOH溶液,其中与OH-反应的离子是H+、Cu2+ | |
| B. | 在②中,固体A中一定含有Ag和Cu,可能含有Fe | |
| C. | 在②中,溶液B的溶质有Ba(NO3)2、Fe(NO3)3 | |
| D. | 废水中含有Ba2+、Ag+、Cu2+、Fe2+、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com