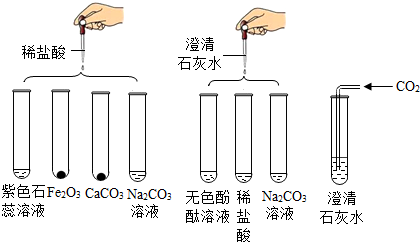
(2012?平顶山二模)某实验小组研究盐酸、氢氧化钙两种物质的化学性质,做了如图所示8个实验.
已知:Na
2CO
3+CaCl
2=CaCO
3↓+2NaCl
(1)若实验后某试管中为黄色溶液,则该试管中发生反应的化学方程式为:
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
.
(2)若实验后某试管中为红色溶液,则向其中加入足量的
稀盐酸
稀盐酸
,溶液变为无色.由此推断,该试管中最初盛有的物质是
无色酚酞试液
无色酚酞试液
.
(3)若实验后某试管的底部有白色固体,且过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现,则该试管中最初发生反应的化学方程为
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
.
(4)实验后某试管中得到无色溶液A,向其中加入足量的Na
2CO
3溶液,无明显现象.由此推断,该试管中最初发生反应的化学方程式为
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
;无色溶液A中的溶质可能是
NaCl或NaCl和Na2CO3
NaCl或NaCl和Na2CO3
.
(5)在实验中发生中和反应的化学方程式为
Ca(OH)2+2HCl=CaCl2+2H2O
Ca(OH)2+2HCl=CaCl2+2H2O
.
(6)若将二氧化碳通入澄清石灰水中,生成5g白色沉淀,过滤后用多少克10%的稀盐酸能将白色沉淀恰好溶解.




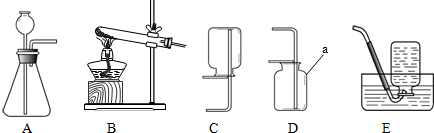
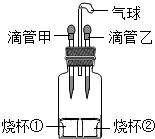 (2012?平顶山二模)如图装置可以完成多个实验,具有药品用量少、现象明显、尾气不外逸等优点.
(2012?平顶山二模)如图装置可以完成多个实验,具有药品用量少、现象明显、尾气不外逸等优点.