
分析 根据硫酸钡的质量求硫酸钠的质量以及生成的氯化钠的质量,注意滤液中溶质的质量是两部分氯化钠,然后根据溶质的质量分数公式,求出所得滤液中溶质的质量分数.
解答 解:设样品中的Na2SO4的质量为x,同时生成NaCl的质量为y
Na2SO4+BaCl2=BaSO4↓+2Na Cl
142 233 117
x 23.3g y
$\frac{142}{x}=\frac{233}{23.3g}=\frac{117}{y}$
x=14.2g
y=11.7g
反应后所得溶液的溶质的质量分数=$\frac{11.7g+(15g-14.2g)}{15g+108.3g-23.3g}×$100%=12.5%
答案:
(1)样品中所含硫酸钠的质量为14.2g;
(2)反应后所得溶液的溶质的质量分数为12.5%.
点评 本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律.本考点主要出现在计算题中.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 烤焦成炭,可以减缓电线杆的腐烂 | B. | 烤焦成炭,可以增加美观 | ||
| C. | 烤焦成炭,可以增强吸附的能力 | D. | 烤焦成炭,可以增强木材的强度 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
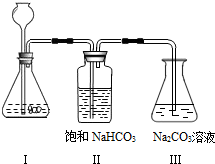
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
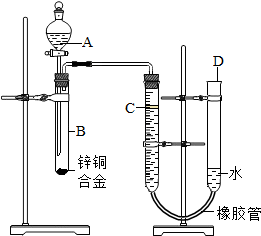 某学习小组用如图所示装置测定锌铜合金中锌、铜的质量分数.
某学习小组用如图所示装置测定锌铜合金中锌、铜的质量分数.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
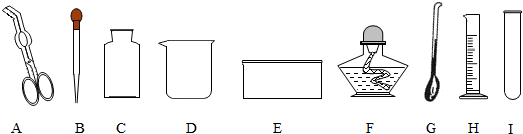
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
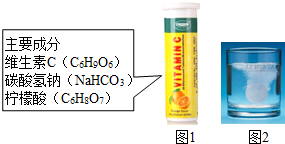 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 构建知识网络是学习和研究化学常用的科学方法,如图是小纪同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.
构建知识网络是学习和研究化学常用的科学方法,如图是小纪同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com