
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量(g) | 25 | 25 | 25 | 25 |
| 生成沉淀的质量(g) | 2.9 | X | 8.7 | 8.7 |
分析 溶液稀释前后,溶质质量不变;
氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)设加入氯化钠的质量为x,蒸发水的适量为y,根据题意有:$\frac{100g×10%+x}{100g+x}$×100%=20%,$\frac{100g×10%}{100g-y}$×100%=20%,
x=12.5g,y=50g,
故填:12.5;50.
(2)由1、2、3可知,25g氢氧化钠溶液和氯化镁反应生成2.9g氢氧化镁沉淀,因此X=5.8,
设氯化镁质量为z,
2NaOH+MgCl2=Mg(OH)2↓+2NaCl,
95 58
z 8.7g
$\frac{95}{z}$=$\frac{58}{8.7g}$,
z=14.25g,
原固体混合物样品中氯化镁的质量分数为:$\frac{14.25g}{20g}$×100%=71.25%,
故填:5.8;71.25%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
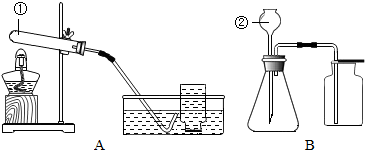
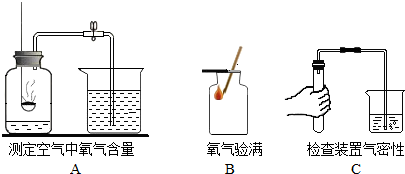
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
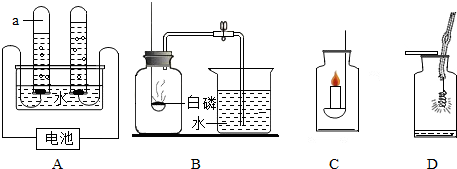
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A环境与健康 | B应用与解释 |
| ①减少酸雨-减少含硫煤的使用 ②减少水污染-合理使用农药、化肥 | ①汽油洗去油污-乳化现象 ②保持铁制菜刀干燥-防止生锈 |
| C灭火与自救 | D性质与用途 |
| ①发现油锅起火-立即用水浇灭 ②煤气泄漏-立即拨打电话求救 | ①氧气可燃性-火箭发射 ②氮气化学性质不活泼-灯泡保护气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:
菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
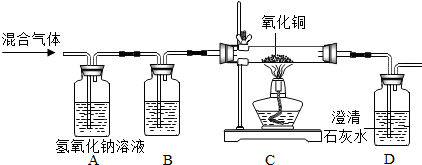
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com