
| 学生甲 | 还可能有Ca(OH)2、NaOH | 学生丙 | 还可能有Ca(OH)2、CaCl2 |
| 学生乙 | 还可能有NaOH、Na2CO3 | 学生丁 | 还可能有Na2CO3 |
| … | … |
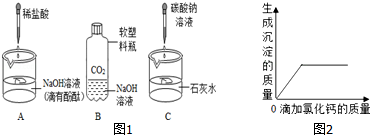
分析 (1)NaOH溶液吸收CO2生成Na2CO3和H2O,据此写出反应的化学方程式.
(2)碳酸钠与石灰水[Ca(OH)2]反应生成碳酸钙沉淀,据此分析实验的现象;
(3)根据试验的各种现象逐一确定各种物质.有沉淀就是CaCO3NaCl是一定的生成物,氢氧化钠能使酚酞变成红色.
解答 解:(1)氢氧化钠能与二氧化碳气体反应生成了碳酸钠和水,化学反应式为:2NaOH+CO2═Na2CO3+H2O;故答为:2NaOH+CO2═Na2CO3+H2O.
(2)碳酸钠与石灰水反应生成碳酸钙沉淀(CaCO3),所以,C试验的现象是:澄清石灰水变浑浊;故答为:澄清石灰水变浑浊.
(3)【假设猜想】废液浑浊是因为碳酸钠溶液与石灰水反应生成了碳酸钙沉淀;稀盐酸与氢氧化钠溶液反应生成了氯化钠,氯化钠不再于其他物质反应.故一定含有:NaCl;由于Ca(OH)2、Na2CO3溶液也可使酚酞试液变红,不能确定是否含有氢氧化钠;故答为:NaCl;Ca(OH)2、Na2CO3溶液也可使酚酞试液变红.
【结论解释】
通过图形可以看出滴加氯化钙后,有沉淀生成,在废液中能与氯化钙反应生成沉淀的只有Na2CO3.故一定含有:Na2CO3;故答为:Na2CO3.
【拓展提高】由于本身混有酚酞,所以可以观察沉淀后的溶液的颜色,若溶液变红,则含有NaOH;若溶液不变色,则不含NaOH.故答为:观察沉淀后的溶液的颜色,若溶液变红,则含有NaOH;若溶液不变色,则不含NaOH.
点评 本题利用各种试验现象推断物质的成分.考查碱在化学反应中的性质.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 19% | B. | 22% | C. | 28% | D. | 20.7% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 菜肴 | 半小时 | 6小时 | 18小时 | 24小时 |
| 炒青菜 | 0.6861 | 0.7982 | 4.3333 | 5.3624 |
| 韭菜炒蛋 | 1.8153 | 1.9249 | 2.8390 | 5.6306 |
| 红烧肉 | 2.4956 | 4.2558 | 4.3668 | 5.5188 |
| 红烧鲫鱼 | ---- | 2.0948 | 3.2300 | 7.2397 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 (1)小明在元素周期表中查找到如图所示的-格后,明白了不能把一氧化碳写成“Co”的原因.
(1)小明在元素周期表中查找到如图所示的-格后,明白了不能把一氧化碳写成“Co”的原因.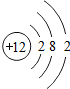 ,Mg原子在化学反应中容易失去(填“得到”或“失去”)2个电子.
,Mg原子在化学反应中容易失去(填“得到”或“失去”)2个电子.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
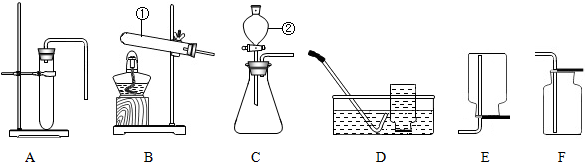
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
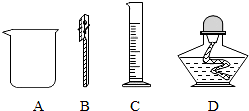
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com