
| 实验 | 温度/ | 反应时间/h | 粗蹄沉淀率 |
| A | 65 | 3.0 | 65.0 |
| B | 80 | 3.0 | 98.9 |
| C | 80 | 2.0 | 98.9 |
| d | 90 | 2.0 | 97.0 |
分析 (1)根据根据质量守恒定律,化学反应前后原子的种类、数目不变解答;
(2)根据表中信息紧系分析解答.
解答 解:(1)TeOSO4+2SO2+3X$\frac{\underline{\;\;△\;\;}}{\;}$Te↓+3H2SO4,反应前有:Te、9O、3S、3X;反应后有:Te、6H、12O、3S,所以3X中含有6H和3O,则每个X分子中含有两个氢原子和一个氧原子,则X 的化学式H2O;
(2)①本实验目的是研究粗碲沉淀率的影响条件,由数据可以知道,本实验研究反应条件是“温度”和“反应时间”这两个条件;
②由实验a 和实验b 对比,反应时间一样,反应的温度不一样,所以通过a 和b 实验目的是“比较相同时间,不同的反应温度对粗碲沉淀率的影响”;
③根据四组实验对比,在温度80℃,反应时间为2.0h 时粗碲的沉淀率最高;
④由表中数据可知,温度为80℃时,不管反应时间是2.0h还是3.0h,粗碲的沉淀率最大都是为98.9%,所以选择A.
答案:
(1)H2O;
(2)①温度、反应时间;
②比较相同时间,不同的反应温度对粗碲沉淀率的影响;
③80、2.0;
④A.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案科目:初中化学 来源: 题型:解答题
| 行星名称 | 行星上“大气”的主要成分 |
| 木星 | 氨气、氦气、氢气、甲烷 |
| 水星 | 没有气体 |
| 冥王星 | 甲烷 |
| 火星 | 二氧化碳 氮气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
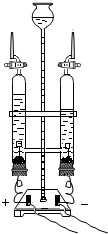 今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.
今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
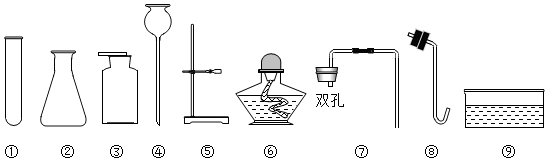
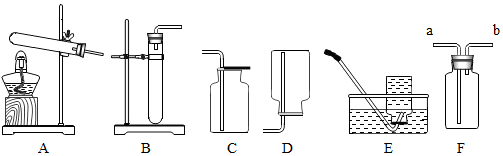
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 | 固体中一定含有 和Ca(OH)2. |
| (2)另取少量固体放于试管中,滴加足量的 | 固体逐渐消失,有无色气体产生,得到浅绿色溶液 | 固体中一定含有Fe,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清石灰水中 | 固体中一定含有CaCO3 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
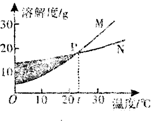
| A. | 30℃时M的溶解度小于N的溶解度 | |
| B. | 分离M、N可采用蒸发结晶的方法 | |
| C. | M、N都是难溶物质 | |
| D. | 阴影处各点对应的溶液(不包含曲线上的点)是N的不饱和溶液,M的饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
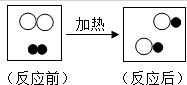 如图为一个化学反应的微观示意图,其中“●”表示H原子,“”表示Cl原子,下列有关说法中正确的是( )
如图为一个化学反应的微观示意图,其中“●”表示H原子,“”表示Cl原子,下列有关说法中正确的是( )| A. | “ ”表示氢分子 ”表示氢分子 | B. | 反应前后分子种类不变 | ||
| C. | 反应涉及二种单质和二种化合物 | D. | 反应可表示为:H2+Cl2=HCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
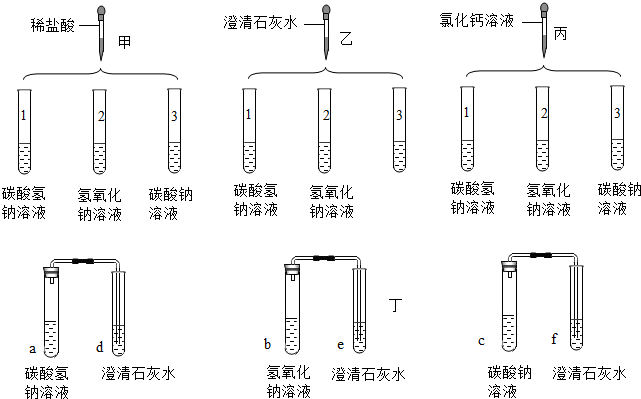
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 为了节约药品将用剩药品放回原试剂瓶 | |
| B. | 实验室制取气体时,应先装药品再检査装置的气密性 | |
| C. | 用排水法收集O2结束时,应先将导管移出水面再停止加热 | |
| D. | 氢气还原氧化铜实验开始时,应先点燃酒精灯再通氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com