


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案科目:初中化学 来源: 题型:
| 400℃-500℃ |
| 500℃-600℃ |
| 700℃-800℃ |

查看答案和解析>>
科目:初中化学 来源: 题型:
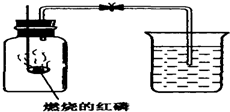 某同学用如图所示装置来测定空气中氧气的体积分数,步骤如下:①用夹子夹紧橡皮管;②点燃燃烧匙中的红磷;③将燃烧匙插入广口瓶并塞上塞子;④燃烧完毕打开夹子.
某同学用如图所示装置来测定空气中氧气的体积分数,步骤如下:①用夹子夹紧橡皮管;②点燃燃烧匙中的红磷;③将燃烧匙插入广口瓶并塞上塞子;④燃烧完毕打开夹子.| 1 |
| 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
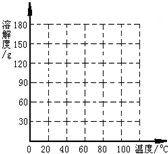 下表是不同温度时KNO3的溶解度数值,根据此表回答下列问题
下表是不同温度时KNO3的溶解度数值,根据此表回答下列问题| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
查看答案和解析>>
科目:初中化学 来源: 题型:

| 仪器编号 | 试剂或装置的作用 | 仪器编号 | 试剂或装置的作用 |
| A | C | ||
| D | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com