
| A. | +1价 | B. | +2价 | C. | +3价 | D. | 无法确定 |
分析 根据题意,金属元素只有一种化合价,结合相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
解答 解:该金属元素A的化合价为x,相对原子质量为y,因为在化合物中,氯元素显-1价,氧元素显-2价.
其与氯元素形成的化合物的化学式为:AClx
金属氧化物的化学式为:A2Ox
又它与氯元素形成的化合物的相对分子质量比它与氧元素形成的化合物的相对分子质量大55,
则y+35.5x-(2y+16x)=55
y=19.5x-55
当x=+1时,y=19.5-55<0(不可能)
当x=+2时,y=19.5×2-55<0(不可能)
当x=+3时,y=19.5×3-55>0
故选:C.
点评 本题难度不大,考查同学们灵活运用化学式的书写与有关计算进行分析问题、解决问题的能力.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
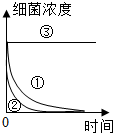 次氯酸钠溶液,俗称漂白水,在烧碱溶液中通入氯气即可制得.漂白水为无色或淡黄绿色液体,
次氯酸钠溶液,俗称漂白水,在烧碱溶液中通入氯气即可制得.漂白水为无色或淡黄绿色液体,| 编号 | 实验目的 | 温度/℃ | pH | 光照/lx |
| ① | 为②③提供对照 | 25 | 5 | 300 |
| ② | 探究温度对杀菌速率的影响 | 10 | 5 | 300 |
| ③ | 探究光强对杀菌速率的影响 | 10 | 5 | 80000 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com