
| A. | 100mL溶质质量分数为40%(密度为1.3g/mL)的硫酸溶液中含硫酸的质量为40g | |
| B. | 30℃时,100g饱和KCl溶液中含 27gKCl,则30C,KCl的溶解度不等于27g | |
| C. | 30℃时100g水中最多溶解37gKCl,则30gKCl饱和溶液中溶质的质量分数为37% | |
| D. | 20℃时硝酸钾溶液的质量分数为5%,可理解为100g硝酸钾溶液中含硝酸钾5g |
分析 A、根据溶质的质量=溶液的质量×溶质质量分数进行分析;
B、根据溶解度的概念进行分析;
C、根据溶质质量分数的计算方法进行分析;
D、根据溶质质量分数的定义进行分析.
解答 解:A、100mL溶质质量分数为40%(密度为1.3g/mL)的硫酸溶液中含硫酸的质量为100mL×1.3g/mL×40%=52g≠40g,故A错误;
B、在一定温度下,某物质在100g溶剂里达到饱和时溶解的质量称为该物质的溶解度,所以30℃时,100g饱和KCl溶液中含27gKCl,则30C,KCl的溶解度不等于27g,故B正确;
C、30℃时100g水中最多溶解37gKCl,则30gKCl饱和溶液中溶质的质量分数为$\frac{37g}{137g}$×100%=27%,故C错误;
D、20℃时硝酸钾溶液的质量分数为5%,可理解为100g硝酸钾溶液中含硝酸钾5g,故D正确.
故选:BD.
点评 本题主要考查了溶质质量分数的计算,难度不大,注意结合定义进行认真分析即可完成.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
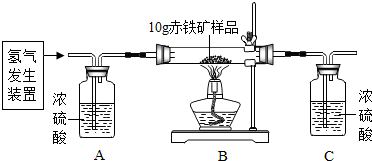
| 装置 | B | C |
| 反应前质量 | 84.3g | 294.1g |
| 反应后质量 | 81.9g | 296.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 锌与稀硫酸反应时加入少量的硫酸铜可以加快产生氢气的速率,等质量的两份锌,向其中加入等质量等浓度且过量的稀硫酸,并向其中一份中加几滴硫酸铜溶液,产生氢气的质量随时间变化图象如图所示.
锌与稀硫酸反应时加入少量的硫酸铜可以加快产生氢气的速率,等质量的两份锌,向其中加入等质量等浓度且过量的稀硫酸,并向其中一份中加几滴硫酸铜溶液,产生氢气的质量随时间变化图象如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | A、B是反应物,C、D是生成物 | |
| B. | B可能是催化剂,A、D一定是生成物 | |
| C. | 反应过程中,当容器中C的质量为8克时,D的质量为6克 | |
| D. | 反应结束后经检验B不存在,则容器中D的质量为22克 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待的做起了这个实验:将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,
小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待的做起了这个实验:将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应.
某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg2+和Fe2+ | B. | Mg2+ Fe2+和Cu2+ | C. | Mg2+和Cu2+ | D. | Fe2+和Cu2+ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 纳米碳质地很柔软,构成其的基本粒子是碳原子 | |
| B. | 纳米氧化锌能吸收电磁波 | |
| C. | 黑色的氧化铜粉末属于纳米材料 | |
| D. | 若将银白色铁通过特殊加工成纳米粉末,其物理性质将发生一定的变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验室制氧气必须用二氧化锰做催化剂 | |
| B. | 工业上采用分离液态空气法制氧气,该过程属于分解反应 | |
| C. | 化学反应前后,催化剂的质量和性质都保持不变 | |
| D. | 当混有高锰酸钾的氯酸钾时,氯酸钾的分解速率会加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com