
分析 (1)根据金属钠的化学性质非常活泼,易与氧气和水发生化学反应分析;
(2)金属钠投入硫酸铜溶液中,根据酚酞试液变红及元素守恒的角度分析钠与水反应的产物并写出方程式;
(3)根据金属钠也能在二氧化碳中燃烧,根据质量守恒定律中化学反应前后元素的种类不变分析黑色固体的成分和白色物质的成分;
方案2:依据滴加足量盐酸,溶液中有气泡冒出,推测白色物质的成分;
方案3:根据加入的试剂与碳酸钠反应出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现,得出合理的猜想的结论,注意在验证是否有氧化钠时,要注意碳酸钠溶液也显碱性,要用氯化钙溶液排除碳酸钠的干扰;
③评价与反思 根据碳酸钠也显碱性分析;
根据金属钠的性质选择合适的灭火方法;
【拓展应用】(1)利用溶质质量=溶液质量×溶质的质量分数,计算配制溶液所需要的溶质的质量和溶剂的质量;由配制一定质量分数的溶液的步骤进行排序;
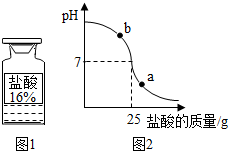
(2)①根据滴加盐酸到图象中a点和b点时溶液发生的反应以及剩余的反应物分析.
②观察图示,当滴加盐酸到C点时,溶液的pH=7,25g的盐酸与20g20%的氢氧化钠溶液恰好完全反应,根据盐酸与氢氧化钠的反应,由氢氧化钠的质量求出所消耗的盐酸中溶质的质量;再根据溶质质量分数的公式计算该盐酸的实际质量分数;
(3)根据盐酸的挥发性分析.
解答 解:(1)金属Na性质活泼,常温下极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠;金属钠还可以与水剧烈反应放出氢气,因此保存在煤油中.
故答案为:防止钠与氧气和水反应变质;
(2)将金属钠投入水中,待反应结束后滴加酚酞溶液,发现溶液变红,说明产生了碱性的物质,根据反应前后元素的种类不变,因此是氢氧化钠;结合资料提供的还产生氢气,因此氧气还能和水反应生成氢氧化钠和氢气;故答案为:2Na+2H2O=2NaOH+H2↑;钠投入硫酸铜溶液中总的化学反应方程式为:
2Na+CuSO4+2H2O═Cu(OH)2+Na2SO4+H2↑; 氧化铜加热后质量又会减少,应该是氧化铜中的氧元素转化为氧气,24g氧化铜的氧元素的质量=24g×$\frac{16}{64+16}$=4.8g,大于2.4g,说明是氧化铜中的部分氧元素转化为氧气,所以此过程中可能发生反应的化学方程式4CuO$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+O2↑.
(3)根据质量守恒定律化学反应前后元素的种类不变可知:二氧化碳和金属钠反应生成了黑色的物质应该是碳和白色的物质不可能是氢氧化钠,因为反应物中无氢元素,因此不可能是氢氧化钠;
方案2:因为滴加足量盐酸,溶液中有气泡冒出,可证明有碳酸钠.
方案3:向滤液中加入过量的某试剂后出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象,说明该试剂能够和碳酸钠反应产生白色沉淀,且反应后的溶液不显碱性,故不能是石灰水和硫酸铜溶液;也说明了白色固体没有水溶液显碱性的氧化钠;故乙的猜想成立;
③评价与反思 向滤液中加入无色酚酞试液,观察到溶液变成红色,不能说明白色物质中一定有氧化钠,因为碳酸钠也显碱性;
结合钠的性质,实验室中的金属钠着火时,不能用水和二氧化碳等棉花,可以采用的灭火方法是用沙子覆盖,与氧气隔绝;
【拓展应用】(1)配制质量分数为20%的氢氧化钠溶液100g,需要氢氧化钠固体的质量为100g×20%=20g,水的质量为:100g-20g=80g,体积为80ml;配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解、装瓶存放,故顺序为:②④①③;需要用到的仪器有:烧杯、玻璃棒、量筒、胶头滴管、托盘天平,
故答案为:20;80;②④①③;玻璃棒;
(2)①由图示可知,当滴加盐酸到图象中a点时,pH<7,说明盐酸的量过量,溶液呈现酸性;当滴加盐酸到图象中b点时,pH>7,说明盐酸的量不足,溶液呈现碱性,部分氢氧化钠参加反应生成了氯化钠,还有剩余的氢氧化钠,所以溶液中的溶质是:NaCl、NaOH;
故答案为:酸;NaCl、NaOH;
②设:此盐酸的质量分数为x
NaOH+HCl=NaCl+H2O
40 36.5
20g×20% 25g×x
$\frac{40}{20g×20%}=\frac{36.5}{25g×x}$
x=14.6%
答:此待测盐酸质量分数为14.6%
(3)盐酸具有挥发性,是导致盐酸溶液溶质质量分数减少的原因;
故答案为:盐酸具有挥发性.
答案:
【问题讨论】
(1)防止钠与氧气反应变质,
(2)2Na+2H2O═2NaOH+H2↑;
2Na+CuSO4+2H2O═Cu(OH)2+Na2SO4+H2↑; 4CuO$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+O2↑
(3)碳(或C)
①反应物中没有氢元素; ②碳酸钠(或Na2CO3); B; 乙;
③碳酸钠溶液也是碱性的; 用黄沙掩埋
【拓展应用】(1)20; 80; ②④①③; 玻璃棒
(2)①酸性; NaOH、NaCl 此待测盐酸质量分数为14.6%
(3)盐酸具有挥发性
点评 本考点属于信息给与题,在主要考查了金属钠的物理性质和化学性质,以及氧气、水和二氧化碳与钠反应的有关性质和反应的类型.还考查了质量守恒定律中,元素的种类反应前后不变,并设计实验,进行探究,能够激发学生的探究欲望,综合性比较强.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | CO(NH2)2 | B. | KCl | C. | Ca(H2PO4)2 | D. | NH4H2PO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用灼烧的方法区别棉花和羊毛 | |
| B. | 用水鉴别NH4NO3、NaOH、NaCl三种固体 | |
| C. | 将草木灰(含K2CO3)与氯化铵混合施用,增进肥效 | |
| D. | 按溶解、过滤、蒸发的主要操作顺序分离CaCl2、CaCO3的固体混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuSO4、NaOH、KNO3、NaCl | B. | K2CO3、NaOH、稀HCl、BaCl2 | ||
| C. | FeCl3、KOH、CaCl2、NaCl | D. | 稀HCl、Na2CO3、H2SO4、Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在实验室用100mL量筒准确量取8.5mL盐酸 | |
| B. | 测定溶液的pH时,将试纸插入待测液中 | |
| C. | 稀释浓硫酸时,将水倒入盛浓硫酸的烧杯中 | |
| D. | 点燃氢气前,一定要先检验氢气的纯度 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 2014年11月4日哈齐客运专线松花江特大桥主体工程完工.松花江上又多了一条连通南北的现代钢铁纽带.下列关于松花江特大桥的有关叙述中正确的是( )
2014年11月4日哈齐客运专线松花江特大桥主体工程完工.松花江上又多了一条连通南北的现代钢铁纽带.下列关于松花江特大桥的有关叙述中正确的是( )| A. | 特大桥上两侧照明灯光应全天开启,有利于车辆通行、美观 | |
| B. | 特大桥建设过程中用的沙子、水泥、钢筋均属于金属材料 | |
| C. | 桥上两侧的金属栏杆上刷油漆,不仅美观而且防锈 | |
| D. | 桥上两边的灯饰外壳采用的塑料属于天然有机高分子材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 11Na 23.00 | 12Mg 24.31 | 13Al 26.98 | 14Si 28.09 |
| A. | Si的相对原子质量是28.09 | |
| B. | Mg原子的核外电子排布是 | |
| C. | Na+的质子数、核外电子数均为11 | |
| D. | 等质量的钠、镁、铝中所含原子个数由多到少的顺序是Na>Mg>Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com