
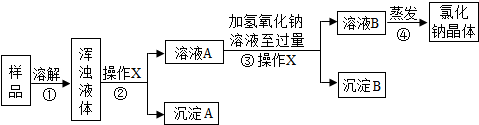
分析 本题属于流程图型除杂质题,还包含了混合物分离中常用的方法,如过滤、蒸发等.一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.在本题中,加入的氢氧化钠溶液会与杂质氯化镁反应生成白色沉淀氢氧化镁.固体与液体分离要用过滤,要得到可溶性固体需要蒸发.由于加入的氢氧化钠溶液是过量的,因此又加入了新的杂质.我们自己设计实验方案时,要用适量的稀盐酸溶液.
解答 解:(1)根据流程图可知:步骤①为溶解,其中玻璃棒搅拌的作用是搅拌,加速溶解;
(2)步骤②、③是固体与液体分离,所以操作X的名称是:过滤;
(3)步骤③中,加入过量氢氧化钠溶液的目的是:使镁离子充分与氢氧根反应生成氢氧化镁沉淀,从而使杂质氯化镁完全除去,氢氧化钠和氯化镁反应会生成氢氧化镁沉淀和氯化钠,化学方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(4)方案步骤③不合理的理由是:加入的氢氧化钠溶液是过量的,则加入了新的杂质,应该采取的措施是:蒸发前,再加入适量的盐酸,调节溶液pH值.
故答案为:(1)搅拌,加速溶解;
(2)过滤;
(3)将杂质氯化镁完全除去,2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(4)加入的氢氧化钠溶液是过量的,则加入了新的杂质;蒸发前,再加入适量的盐酸,调节溶液pH值.
点评 本考点属于物质的分离和提纯,还考查了混合物的分离方法,是中考的重点也是一个难点.本题利用流程图中的现象和实验方案的设计,考查同学们的判断能力,同学们只要认真分析,根据条件综合把握,问题就会迎刃而解.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在氧气中燃烧产生蓝紫色的火焰 | B. | 铁丝在氧气中燃烧火星四射 | ||
| C. | 蜡烛在空气中燃烧产生大量白烟 | D. | 木炭在氧气燃烧发出白光 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用5mL水和5mL酒精混合,可配制成10mL酒精溶液 | |
| B. | 用托盘天平称取5.62 g氧化铜粉末 | |
| C. | 用pH试纸测定某酸性溶液,pH值为5.4 | |
| D. | 用10 mL量筒量取8.2 mL水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
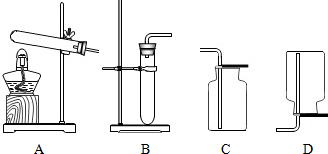 实验室提供了以下药品和装置(如图所示),请回答问题.
实验室提供了以下药品和装置(如图所示),请回答问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.
图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com