
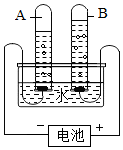
 如图是电解水的实验装置,通电后,两电极上都有气体放出.
如图是电解水的实验装置,通电后,两电极上都有气体放出.分析 根据电解水时,与正极相连的试管产生的是氧气,与负极相连的试管产生的是氢气,氧气和氢气的体积比约为1:2解答.
解答 解:
(1)根据电解水时,与电源负极相连的试管产生的气体是氢气,能够燃烧,氢气燃烧时能够发出淡蓝色火焰;与正极相连的试管产生的是氧气,用带火星的火柴检验,产生的现象是:能使带火星的木条复燃,说明气体具有助燃性,则该气体为氧气;氧气和氢气的体积比约为1:2.
(2)水在通电的条件下分解为氢气和氧气;电解水实验说明,水是由氢元素和氧元素组成的.文字表达式为:水$\stackrel{通电}{→}$氢气+氧气.
故答案为:
(1)带火星的木条复燃;氧气;
(2)氢元素和氧元素;水$\stackrel{通电}{→}$氢气+氧气
点评 解答本题要掌握电解水的知识,只有这样才能对电解水方面的问题做出正确的判断.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:初中化学 来源: 题型:解答题
| 实验混合溶液 | A | B | C | D | E | F |
| 28%稀盐酸/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| HO/mL | V7 | V8 | V9 | V10 | 8 | 0 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 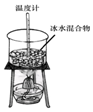 冰熔化过程中冰水混合物温度高于0℃ | |
| B. |  冷冻室取出的冰棍,外表的“霜”是由空气中水蒸气凝华而成 | |
| C. |  通常采用降温的方法将石油气液化储存在钢罐内 | |
| D. |  舞台上的云雾是干冰升华成的二氧化碳气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
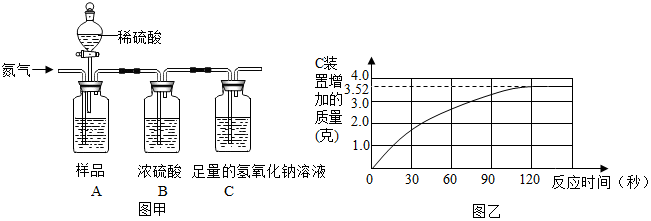
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
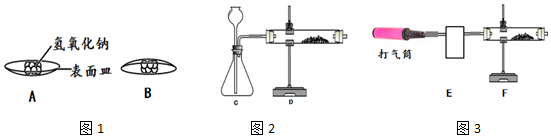
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化 | B. | 还原 | C. | 催化 | D. | 分解 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该气体可能含有CH4和H2 | B. | 该气体一定含有H2和CO | ||
| C. | 该气体可能含有CO和CH4 | D. | 该气体可能含有H2、CO、CH4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 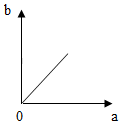 | B. | 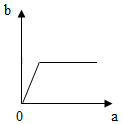 | C. |  | D. | 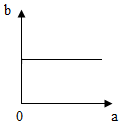 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com