
分析 (1)根据葡萄糖的化学式的写法,有机物的概念,硫酸铜与氢氧化钠反应原理进行回答;
(2)根据氧化亚铜能与酸反应,得到+2价的铜盐和单质铜;在空气中灼烧氧化亚铜和铜均生成氧化铜进行回答;
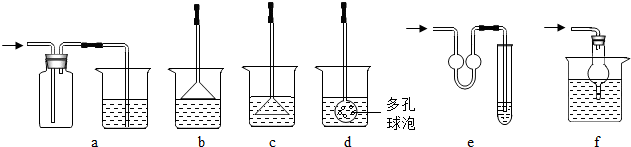
(3)根据反应条件选择气体发生装置;
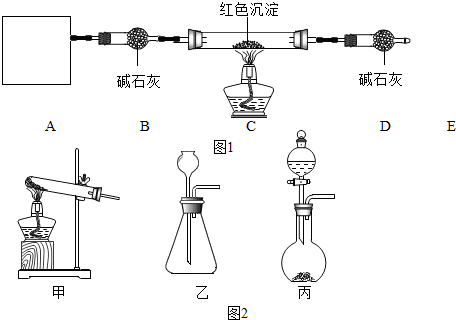
(4)根据碱石灰为氢氧化钠和氧化钙的混合物能吸收水分及反应发生前后通入氨气的作用分析作答;
(5)通过分析有利于气体吸收的方法措施进行解答;
(6)通过计算分析说明;
(7)根据氧化铜和氨气的反应可以知道,在反应前后氧化铜失去了氧,而氧化铜失去的氧和生成的水中的氧元素的质量相等,而D装置吸收了水分,所以实验前后增加的质量即为生成水的质量,而水是由氢氧两种元素组成的,所以结合氧元素的质量可以计算出氢元素的质量,进而计算出氢氧两种元素的质量比;
(8)根据红色沉淀未完全干燥,D管质量增大值偏高分析作答.
解答 解:(1)葡萄糖的化学式为C6H12O6;属于有机物;检验葡萄糖用的新制氢氧化铜由硫酸铜溶液与氢氧化钠溶液反应生成,反应的化学方程式为:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓;
(2)根据查阅资料,写出氧化亚铜与稀硫酸的反应方程式为:Cu2O+H2SO4═Cu+CuSO4+H2O; 取该红色沉淀加入稀盐酸中,①Cu2O与②Cu2O和 Cu均会使溶液变蓝,故方案1不合理;由于Cu2O+H2SO4═Cu+CuSO4+H2O,取该红色沉淀溶于足量的稀硫酸中,观察到有残渣无法区分①Cu2O与②Cu2O,故方案2不合理;Cu2O和 Cu在空气中充分灼烧均可完全变成黑色氧化铜,但增重比例不同,所以方案3:称取红色沉淀a g,在空气中充分灼烧至完全变黑,并在干燥器里冷却,再称重,反复多次直到固体恒重,称得质量为b g,比较a,b关系是合理的;故填:方案3;
(3)A处为用浓氨水与固体CaO接触,以产生稳定持续的氨气,属于固液反应无需加热型,则A处的发生装置应选图2的丙;
(4)碱石灰可以吸收水蒸汽;因为氨气是碱性气体,在本装置中,增加装有碱石灰的干燥管③,用来吸收氨气中的水蒸汽,减少对实验结果的影响;加热前先通氨气的目的除了消除掉原来空气的二氧化碳和水蒸汽对实验结果影响,还具有一个作用是作保护气,防止红色固体加热时被空气中氧气氧化;停止加热,继续通氨气除了让生成的铜充分冷却,还有的一个作用为让生成的水蒸汽被完全吸收;
(5)增大接触面积和接触时间仅有利于反应的发生,为防止未反应的氨气扩散到空气中,E处可以连接的装置为bef;
(6)反应中生成水的质量是:111.9g-108.3g=3.6g,
设参加反应的Cu2O的质量为x,
2NH3+3Cu2O═N2+6Cu+3H2O
432 54
x 3.6g
$\frac{432}{54}$=$\frac{x}{3.6g}$
解得:x=28.8g
所以红色沉淀的成份为氧化亚铜;
(7)根据氧化铜和氨气的反应可以知道,在反应前后氧化铜失去了氧,而氧化铜失去的氧和生成的水中的氧元素的质量相等,所以还需要测出一个数据,你认为要测出的数据为完全反应后玻璃管中固体质量;故选C;
(8)红色沉淀未完全干燥,D管吸收水分质量增大值偏高,计算水中氢.氧元素的质量比时氧元素的比数就会偏高,会使测定水中氢.氧元素的质量比偏小,故选B.
故答案为:(1)C6H12O6;有机物;2NaOH+CuSO4═Na2SO4+Cu(OH)2↓;
(2)Cu2O+H2SO4═Cu+CuSO4+H2O;方案3;
(3)丙;
(4)除去水蒸汽;防止红色固体加热时被空气中氧气氧化;让生成的水蒸汽被完全吸收;
(5)bef;
(6)氧化亚铜;
(7)C;(8)B.
点评 同学们要具有综合的化学知识才能做好此题.


科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水等于氢气和氧气 | |
| B. | 每2份质量的水在通电条件下生成2份质量的氢气和1份质量的氧气 | |
| C. | 2个水分子生成2个氢气和1个氧气 | |
| D. | 水在通电条件下分解生成氢气和氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com