
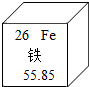
 元素周期表中铁元素的某些信息如图所示,下列有关铁的说法不正确的是( )
元素周期表中铁元素的某些信息如图所示,下列有关铁的说法不正确的是( )| A. | 原子核内有26个质子 | B. | 相对原子质量为55.85 | ||
| C. | 是地壳中含量最多的金属元素 | D. | 是金属元素 |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可.
解答 解:A、根据元素周期表中的一格可知,左上角的数字为26,表示原子序数为26;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为26,故选项说法正确.
B、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为55.85,故选项说法正确.
C、铝是地壳中含量最多的金属元素,故选项说法错误.
D、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是铁,属于金属元素,故选项说法正确.
故选:C.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力.


科目:初中化学 来源: 题型:选择题
| A. | 为治理雾霾,禁止使用化石燃料 | |
| B. | 变废为宝,将地沟油转化成航空燃料 | |
| C. | 城市道路使用太阳能景观灯,节能又环保 | |
| D. | 使用电动汽车,减少尾气排放,改善空气质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
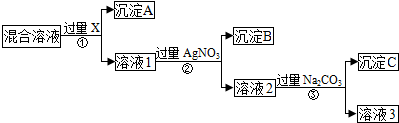
| A. | 试剂X可能是Ba(NO3)2或Ba(OH)2 | |
| B. | 溶液3中含有的溶质是NaNO3和Na2CO3 | |
| C. | 沉淀A、B、C分别是BaSO4、AgCl和BaCO3 | |
| D. | 向溶液3中滴加稀硝酸溶液呈中性,即得NaNO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某兴趣小组甲为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组甲为验证质量守恒定律,做了镁条在空气中燃烧的实验.| 实验操作 | 实验现象及结论 |
| 1 取少量黄色固体于试管中,加入适量的水 ②滴加酚酞试液 | 现象:①产生有刺激性气味的气体 ②酚酞试液变红色 结论:证明猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 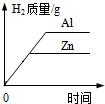 等物质的量且大小相同的锌片、铝片分别与足量且质量分数相同的稀硫酸反应 | |
| B. | 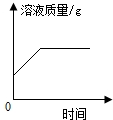 一定量锌片放入硫酸亚铁溶液中 | |
| C. | 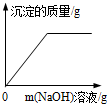 向CuCl2和HCl的混合溶液中滴加NaOH溶液 | |
| D. |  向饱和的硫酸铜溶液中加入硫酸铜粉末 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
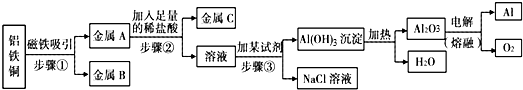
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com