
某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体)。实验过程如下:
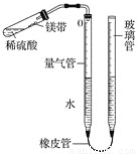
①取一段镁带样品,准确称得其质量为0.030 g;
②往量气管内装水至低于刻度“0”的位置,如图所示,(未装药品)装配好仪器;
③_________________________;
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞;
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置;
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应;
⑦待冷却至室温后,再次记录量气管中液面位置;
⑧算出量气管中增加的气体体积为23.96 mL;
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和。
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式:____________________。
(2)能否用托盘天平称量0.030 g镁带样品________(填“能”或“不能”)。
(3)操作③是_________________________。
(4)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果________(填“是”或“否”),理由是_______________________。
(5)若实际测得氢气的体积与理论值相比偏大,则可能的原因是________________________。
Mg+H2SO4===MgSO4+H2↑ 不能 检查装置的气密性 否 因为残留的氢气体积等于从试管中排出的空气体积,对实验结果无影响 未冷却至室温就记录量气管中液面位置 【解析】(1)根据锌与硫酸反应生成硫酸锌和氢气解答;(2)根据托盘天平的精确度解答;(3)根据由气体生成和参加的反应必须检查装置气密性解答;(4)根据残留的氢气体积等于从试管中排出的空气体积解答;(5)根据实验操作步骤分析解... 习题精选系列答案
习题精选系列答案科目:初中化学 来源:山东省乐陵市2017-2018学年八年级下学期月考化学试卷 题型:综合题
如图是初中化学中的一些重要试验,请回答;










查看答案和解析>>
科目:初中化学 来源:河南省原名校2018届九年级考第四次大联考化学试卷 题型:简答题
向盛有少量碳酸钾溶液的试管里滴入澄清石灰水。
(1)康康同学在配制该碳酸钾溶液时,量取水时俯视读数,则会导致溶液浓度如何变化____?
(2)加入澄清石灰水的过程中,溶液中的溶质可能是:氢氧化钾和氢氧化钙;氢氧化钾;你的猜想是什么_______________?
(3)请设计实验验证你的猜想_____________。(简要写出实验步骤现象和结论)
偏大。 碳酸钾和氢氧化钾。 取少量样品,加入足量CaCl2溶液(或BaCl2溶液等),有沉淀产生,证明有K2CO3;静置,向上层清液中滴加几滴酚酞溶液,溶液变成红色,证明有KOH。 【解析】(1) ,在配制该碳酸钾溶液时,量取水时俯视读数,则导致量取水的量偏少,则会导致溶液浓度偏大;(2)氢氧化钙和碳酸钾反应生成碳酸钙沉淀和氢氧化钾,加入澄清石灰水的过程中,分析反应后的成分时,除考虑生成物外...查看答案和解析>>
科目:初中化学 来源:河南省原名校2018届九年级考第四次大联考化学试卷 题型:单选题
下列化学方程式符合题意且书写正确的是
A. 正常雨水的pH约为5.6的原因:SO2+H2O=H2SO3
B. 医疗上用氢氧化铝治疗胃酸过多:Al(OH)3+3HCl=AlCl3+3H2O
C. 用稀硫酸除铁锈:H2SO4+FeO=FeSO4+H2O
D. 证明铜的活动性比银强:Cu+2AgCl=CuCl2+2Ag
B 【解析】A. 正常雨水的pH约为5.6的原因:CO2+H2O=H2CO3,错误;B. 医疗上用氢氧化铝治疗胃酸过多:Al(OH)3+3HCl=AlCl3+3H2O,正确;C. 用稀硫酸除铁锈:Fe2O3+3H2SO4= Fe 2(SO4)3+3H2O,错误;D. 可利用金属和盐溶液的反应证明铜的活动性比银强,但是氯化银是沉淀,和铜不反应,错误。故选B。查看答案和解析>>
科目:初中化学 来源:厦门市翔安区2018届九年级中考复习模拟卷化学试卷 题型:简答题
古代湿法炼铜的反应原理是:Fe+CuSO4= FeSO4+Cu,若得到16kg的铜,理论上需要铁质量是多少?
【解析】
设铁的质量为x。

56/64=x/16
x=14Kg
答:理论上需要铁的质量是14kg。
本题在解题过程中格式有什么错误?请指出错误并改正。______________
解题中所列的已知量没有单位,应该为16kg 【解析】认真检查解题过程,发现问题。通过检查,x不写单位,没问题,发现解题中所列的已知量没有单位,应该为16kg。查看答案和解析>>
科目:初中化学 来源:厦门市翔安区2018届九年级中考复习模拟卷化学试卷 题型:填空题
下列物质中,属于纯净物的有_____________,属于混合物的有____________
①海水、②糖水、③洁净的空气、④氧化镁、⑤白酒、⑥液态氧、⑦红磷、⑧加碘食盐、⑨可乐饮料、⑩食醋。
④⑥⑦ ①②③⑤⑧⑨⑩ 【解析】利用纯净物和混合物的概念来判断,物质是否为纯净物,宏观上看只有一种物质,微观上只有一种分子,否则属于混合物。①海水中含有氯化钠、氯化镁、水等物质,属于混合物;②糖水中含有糖和水,属于混合物;④洁净空气中含有氧气、氮气、二氧化碳等物质,属于混合物;④氧化镁是由一种物质组成,属于纯净物;⑤白酒中含有酒精和水,属于混合物;⑥液态氧是氧气的液态,属于纯净物;⑦红磷由一...查看答案和解析>>
科目:初中化学 来源:厦门市翔安区2018届九年级中考复习模拟卷化学试卷 题型:填空题
如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图回答下列问题。

(1)t1℃时,溶解度最大的物质是 。
(2)若将M点处C的不饱和溶液变成饱和溶液,可以选择的方法是 (填序号)。
A.降低温度 B.增加溶质 C.蒸发溶剂
(3)t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发) 。
(1)C (2)BC (3)A=C<B 【解析】试题根据溶解度曲线的含义可知(1)t1℃时,溶解度最大的物质是溶解度曲线最高的物质C;(2)若将M点处C的不饱和溶液变成饱和溶液,因为物质C的溶解度随温度的升高而减小,故可以选择的方法是升高温度,增加溶质、蒸发溶剂;故选择BC; (3)t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,t2℃时AC的溶解度数值相等且大于B物质,故溶液中溶剂...查看答案和解析>>
科目:初中化学 来源:厦门市翔安区2018届九年级中考复习模拟卷化学试卷 题型:单选题
某工厂的废渣中混有少量的锌粉和氧化铜(其他的成分不与酸反应),这些废渣与废盐酸接触时就会形成污水,造成公害。若向污水中撒入铁粉,且反应后铁粉过量,此时,污水中一定含有的金属离子是( )
A. Fe2+、Cu2+
B. Cu2+、H+
C. Zn2+、Fe2+
D. Zn2+、H+
C 【解析】当少量的氧化铜和锌粉混合后氧化铜与锌都可以与盐酸反应生成氯化锌和氯化铜。铁的活动性比铜强所以可以置换出氯化铜溶液中的铜而生成氯化亚铁,且由于铁粉过量,铁会与污水中可能存在的盐酸反应,生成氯化亚铁,所以溶液中一定不会存在氯化铜和盐酸,由于铁的活动性比锌弱所以不会置换出氯化锌溶液中的锌,所以溶液中一定含有的溶质是ZnCl2、FeCl2,因此溶液中含有的金属离子是Zn2+、Fe2+。故...查看答案和解析>>
科目:初中化学 来源:山东省菏泽市2018年中考化学试卷 题型:单选题
类比推理在化学学习和科学研究中有重要意义,下列说法正确的是
A. 化合物中含不同种元素,所以含不同种元素的物质都是化合物
B. CO2和SO2都能与碱溶液反应,所以非金属氧化物一定能与碱溶液反应
C. 碱的溶液显碱性,显碱性的溶液一定是碱溶液
D. 同种元素的原子所含质子数相同,含有相同质子数的微粒不一定属于同种元素
D 【解析】A、化合物中含不同种元素,含不同种元素的物质不一定都是化合物,也可能是混合物,故选项推理错误;B、CO2和SO2都能与碱溶液反应,但非金属氧化物不一定能与碱溶液反应,如一氧化碳不能与碱溶液反应,故选项推理错误;C、碱的溶液显碱性,显碱性的溶液不一定是碱溶液,也可能是碳酸钠等盐溶液,故选项推理错误;D、同种元素的原子所含质子数相同,含有相同质子数的微粒不一定属于同种元素,可能是原子...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com