


科目:初中化学 来源: 题型:阅读理解
| ||
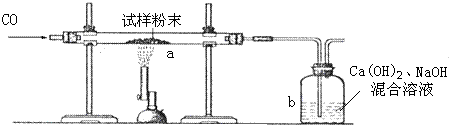
| 反应前 | 反应后 | |
| a管 | 玻璃管和试样粉末的总质量为70.0g | 玻璃管和固体物质的总质量为67.6g |
| b瓶 | 洗气瓶和所盛溶液的总质量为200.0g | 洗气瓶和瓶中物质的总质量为206.6g |
查看答案和解析>>
科目:初中化学 来源:黄冈重点作业·初三化学(下) 题型:022
选择适当的化学试剂或方法,将下列物质中的杂质除去(括号内物质为杂质).
(1)氧气(水蒸气)________________________________
(2)氧化铜(碱式碳酸铜)__________________________
(3)食盐水(泥沙)________________________________
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:2005年山西省中考化学模拟试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com