(2009?吴中区一模)(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以a小题计分.)
a.在实验室易燃品橱柜里有瓶失去标签的试剂,某同学为探究其成分,进行如下实验分析:取2.16g该物质,使其完全燃烧,测知只生成2.16g水和5.28g二氧化碳,请你计算后填空:
(1)该物质中含氢元素______ g,含碳元素______g.
(2)该物质中______ (填“含”或“不含”)有氧元素;若含有氧元素,则氧元素质量为______ g(若不含氧元素,此空不填).
b.“亮菌甲素化学式为C12H10O5,是黄色或橙黄色结晶粉末,几乎不溶于水,辅料为丙二醇(C3H8O2),溶成针剂用于临床.该药为利胆解痉药,适用于急性胆囊炎、慢性胆囊炎急性发作及慢性浅表性胃炎等.试计算:
(1)“亮菌甲素”的相对分子质量为______;
(2)“亮菌甲素”中C、H、O三种元素的质量比为______;
(3)78g“亮菌甲素”完全燃烧时消耗氧气______g.
【答案】
分析:a、根据元素的质量分数的求法,来反向求出氢、氧元素的质量,然后利用质量守恒定律来判断是否含有氧元素,并求出其质量;
b、(1)根据化学式求出其相对分子质量;
(2)元素的质量比等于其相对原子质量和的比;
(3)根据化学方程式可以求出氧气的质量.
解答:解:a、根据分析可以知道水中氢元素和二氧化碳中的碳元素全部来自于该未知的物质中,故可以求出氢元素和碳元素的质量,氢元素的质量=2.16g×
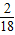
×100%=0.24g;碳元素的质量=5.28g×
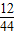
×100%=1.44g;由于1.44g+0.24g=1.68g<2.16g,根据质量守恒定律可以知道该物质中含有氧元素,其质量为:2.16g-1.68g=0.48g;
b、(1)物质的相对分子质量等于各原子的相对原子质量乘以其原子个数,故“亮菌甲素”的相对分子质量为:12×12+1×10+16×5=234;
(2)该物质中各元素的质量比为:(12×12):(1×10):(16×5)=72:5:40;
(3)设消耗氧气的质量为x,则:
C
12H
10O
5+12O
2
12CO
2+5H
2O
234 384
78g x

解得:x=128g.
故答案为:a、0.24g;1.44g;含;0.48g;
b、(1)234;
(2)72:5:40;
(3)128g.
点评:能够熟练的运用质量守恒定律来对物质的成分进行判断,并能够根据化学方程式进行计算.

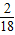 ×100%=0.24g;碳元素的质量=5.28g×
×100%=0.24g;碳元素的质量=5.28g×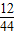 ×100%=1.44g;由于1.44g+0.24g=1.68g<2.16g,根据质量守恒定律可以知道该物质中含有氧元素,其质量为:2.16g-1.68g=0.48g;
×100%=1.44g;由于1.44g+0.24g=1.68g<2.16g,根据质量守恒定律可以知道该物质中含有氧元素,其质量为:2.16g-1.68g=0.48g; 12CO2+5H2O
12CO2+5H2O



 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O