
| 170 |
| x |
| 58.5 |
| y |
| 143.5 |
| 14.35g |
| 17g |
| 170g |


 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:初中化学 来源: 题型:
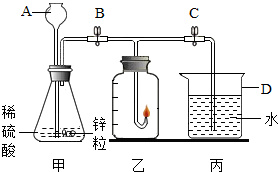 (2005?贵阳)某化学兴趣小组的同学准备用氢气燃烧法测定空气中氧气的体积分数,设计的实验装置如图:
(2005?贵阳)某化学兴趣小组的同学准备用氢气燃烧法测定空气中氧气的体积分数,设计的实验装置如图:| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com