
实验室利用下列反应原理制取氧气,不合理的是
A.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
B.2H2O2![]() 2H2O+O2↑
2H2O+O2↑
C.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
科目:初中化学 来源: 题型:阅读理解
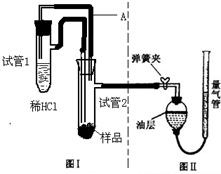 轻质碳酸镁(化学式为4MgCO3?Mg(OH)2?4H2O)是制取氧化镁、颜料、油漆、日用化妆品的工业原料.
轻质碳酸镁(化学式为4MgCO3?Mg(OH)2?4H2O)是制取氧化镁、颜料、油漆、日用化妆品的工业原料.
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
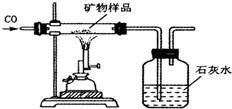 已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首.
已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首.查看答案和解析>>
科目:初中化学 来源: 题型:
| 氢氧化钠 体积:500mL 化学式:NaOH 相对分子质量:40 密度:1.5 g/cm3 质量分数:50%(1)用20mL氢氧化钠溶液可以配制质量分数为10%的氢氧化钠溶液 (2)利用刚配制好的氢氧化钠除去混有RCl2的NaCl固体(R代表某二价金属).取20g该固体样品,全部溶解在100g水中,再加入刚配制好的溶液80g,混合到恰好完全反应后过滤,得到固体的质量为9.8g. ①题中发生反应的化学方程式为 ②利用已知条件求解反应生成NaCl质量(x)的比例式为 ③R的元素符号是 ④原混合物中NaCl的质量分数为 ⑤向反应后所得溶液中加入173.8g水,则此时溶液中溶质的质量分数是 查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 某研究性学习小组,从下列装置中选用部分装置组装后在实验室里制取氧气,并通过排水量来测定所收集到氧气的体积. 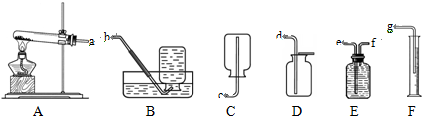 (1)甲同学用一定质量的高锰酸钾制取氧气,反应的化学方程式为 2KMnO4
2KMnO4 ,整套实验装置接口的正确连接顺序为a→
f f →e e →g g .(2)实验过程中,甲同学观察到E装置中的水变为紫红色,这是因为 高锰酸钾粉末 高锰酸钾粉末 进入E装置并溶于水中的缘故.为了防止实验过程中出现上述现象,相应的改进措施是在试管口放一团棉花 在试管口放一团棉花 .(3)实验结束,乙同学意外发现收集到的氧气体积大于理论值,为此继续进行以下实验探究: 提出问题:出现“收集到的氧气体积大于理论值”的原因是什么? 作出猜想:猜想Ⅰ:可能是反应生成的二氧化锰分解放出氧气; 猜想Ⅱ:可能是反应生成的锰酸钾分解放出氧气; 猜想Ⅲ: 可能是锰酸钾和二氧化锰均被分解放出氧气 可能是锰酸钾和二氧化锰均被分解放出氧气 .请回答他做出猜想Ⅲ的理由是锰酸钾和二氧化锰都含有氧元素 锰酸钾和二氧化锰都含有氧元素 .实验验证: 实验一:取一定质量的二氧化锰于试管中,加热一段时间,冷却后测得固体残留物的质量不变.证明猜想 Ⅰ和Ⅲ Ⅰ和Ⅲ 错误.实验二:取一定质量的锰酸钾于试管中,加热一段时间 冷却后测得固体残留物的质量较原固体减少 冷却后测得固体残留物的质量较原固体减少 .综合实验一和实验二,证明猜想Ⅱ正确.反思拓展:实验结束后,经过讨论、交流,丙同学用下列仪器和药品又设计了一个实验方案测定空气中氧气的体积分数. ①带瓶塞的1000mL圆底烧瓶 ②电子天平(称量精确度为0.01g) ③酒精灯 ④某种较活泼的金属粉末(实验过程中需要用到的其他实验用品已省略,实验中有关物质的物理量数据为已知)他的实验步骤是: 先用电子天平称出稍过量的金属粉末的质量,再把金属粉末放在带瓶塞的1000mL的圆底烧瓶中灼烧,至氧气完全反应; 先用电子天平称出稍过量的金属粉末的质量,再把金属粉末放在带瓶塞的1000mL的圆底烧瓶中灼烧,至氧气完全反应; _再称量反应后圆底烧瓶中固体物质的质量;最后通过密度公式求氧气的体积 再称量反应后圆底烧瓶中固体物质的质量;最后通过密度公式求氧气的体积 .再利用实验数据和已知数据就可换算得出空气中氧气的体积分数.查看答案和解析>> 科目:初中化学 来源: 题型: 某研究性学习小组欲利用下列装置进行气体制取的探究,请你分析并填空. 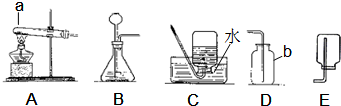 (1)实验室用氯酸钾取氧气,应选择的发生装置是 (2)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集干燥的甲烷应选择的装置组合是 (3)实验室用B和D的组合来制取二氧化碳,写出该反应的化学方程式 (4)工业上二氧化碳是由石灰石高温煅烧而成(已知:CaCO3
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |