
 某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你一起对此展开探究.
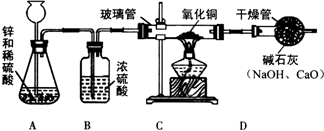
某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你一起对此展开探究.分析 锌能和稀硫酸发生置换反应,浓硫酸具有吸水性;
空气中含有水和二氧化碳;
玻璃管中固体减少的质量就是生成的水中氧元素的质量,红色固体a中含有Cu2O不影响对水的测定结果;
玻璃管的质量,反应前后红色固体a和玻璃管的总质量都已经称量,如果再知道生成水的质量,就可以确定红色固体a的成分;
根据化学方程式计算可以确定红色固体a的成分.
解答 解:【设计方案】
锌和稀硫酸反应能生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
故填:Zn+H2SO4═ZnSO4+H2↑.
洗气瓶B中浓硫酸的作用是吸收水.
故填:吸收水.
【实验探究】
用此数据算得水中氧元素的质量是1.6g,氢元素的质量是1.82g-1.6g=0.22g,则水中H、O元素的质量比为:0.22g:1.6g=11:80,由水的化学式算得H、O元素的质量比为:
(1×2):(16×1)=1:8.
故填:11:80;1:8.
【分析交流】
因为空气中的水、二氧化碳进入了干燥管,影响了结果,所以应该在D装置后面再连接一个干燥管,这样能够防止空气中的水和二氧化碳进入D中.
故填:在D装置后面再连接一个干燥管.
【分析交流】
红色固体a中含有Cu2O不影响水测定结果,因为玻璃管中固体减少的质量就是生成的水中氧元素的质量,和固体的成分无关.
故填:不影响.
【提出猜想】猜想②应该是氧化亚铜.
故填:Cu2O.
【拓展猜想】
因为完全反应后铜的质量通过称量可以计算出来,如果知道反应生成的水的质量,根据化学方程式可以求出反应生成铜的质量,再和通过称量计算出的铜的质量比较,就可以确定固体的组成,因此还需要称量反应后红色固体a和玻璃管的质量.
故填:反应后红色固体a和玻璃管.
【定量分析】
设3.6g红色固体a都是Cu2O,则完全反应后生成铜的质量为X,
Cu2O+H2SO4=CuSO4+Cu+H2O
144 64
3.6g X
$\frac{144}{64}=\frac{3.6g}{X}$
X=1.6g,
与得到的红色固体2g不符,说明红色固体中含有氧化亚铜和铜.
故填:1.6;①.
点评 通过计算可以确定物质的组成,这是近年来常考的内容之一,既是重点、又是难点,要仔细领会、全面掌握.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 8.4g 铝 | B. | 8.4g氧化钙 | C. | 8.4g 锌 | D. | 8.4g碳酸镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
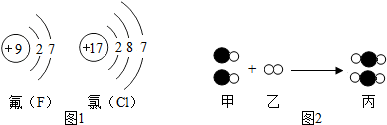
 ”和“
”和“ ”分别表示不同元素的原子).甲、乙、丙三种物质中属于单质的是乙;甲和丙两种物质化学性质不同的原因是分子构成不同.
”分别表示不同元素的原子).甲、乙、丙三种物质中属于单质的是乙;甲和丙两种物质化学性质不同的原因是分子构成不同.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 拒绝使用一次性木筷 | |
| B. | 将废纸、饮料瓶等收集起来,一次性焚烧 | |
| C. | 选择自行车作为出行工具 | |
| D. | 控制农药、化肥的用量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com