
| A、茶氨酸属于有机化合物 |
| B、茶氨酸由26个原子构成 |
| C、茶氨酸中氢元素的质量分数最大 |
| D、茶氨酸中碳、氢、氧、氮元素的质量比为7:14:3:2 |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
| A、丙氨酸不是有机物 |
| B、丙氨酸中碳、氢、氧、氮元素的质量比为36:7:16:14 |
| C、丙氨酸是由碳原子、氢原子、氧原子和氮原子多原子分子构成的化合物 |
| D、丙氨酸是形成蛋白质的一种氨基酸,该物质中含有13个原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、食品包装时充氮以防腐 |
| B、用甲醛溶液浸泡海产品 |
| C、食盐腌渍蔬菜、鱼、肉等 |
| D、合理使用农药,减少果蔬中农药残留 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、Fe3+、SO42-、H+ |
| B、NH4+、K+、NO3- |
| C、Na+、CO32-、Cl- |
| D、Mg2+、SO42-、NO3- |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样,加适量水,搅拌,过滤 ②取少量滤液于试管中,滴入酚酞 试液 ③取少量滤渣于试管中,加入盐酸 |
② ③ |
猜想一成立 |
| 加入盐酸溶液的质量/g | 0 | 4 | 7.3 | 12 |
| 样品的pH | 12 | 9 | 7 | 4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
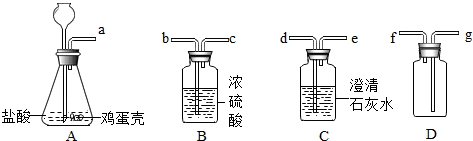
查看答案和解析>>
科目:初中化学 来源: 题型:
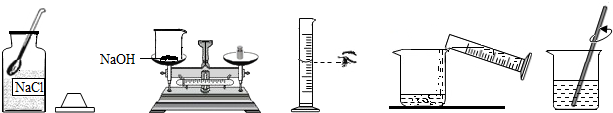
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com