
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:阅读理解
 15、某化学课外兴趣小组,开展了以下两项活动:
15、某化学课外兴趣小组,开展了以下两项活动: 实验过程中溶液的pH变化曲线如右图所示:
实验过程中溶液的pH变化曲线如右图所示:查看答案和解析>>
科目:初中化学 来源:九年级化学-对“探究空气中氧气的体积分数”试题的分析、反思与实践 题型:022
| |||||||||||||||||||
查看答案和解析>>
科目:初中化学 来源:精编教材全解 化学 九年级 上册 沪教版 题型:059
某研究性学习小组设计了如图所示的装置,探究空气中氧气的体积分数,其中A是标有以cm为单位的刻度尺、且在0刻度正上方一圆状缺口处有一圆筒状玻璃容器(带橡皮塞B),C为能自由移动的活塞.
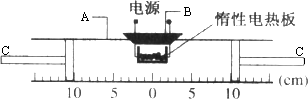
他们操作过程如下:
a.检查装置的气密性;
b.将两个可自由移动的活塞C分别调整到左右两边刻度的10 cm处;
c.将过量的铜粉平铺在惰性电热板上,塞上橡皮塞B;
d.通电加热铜粉,待充分反应后,冷却到原来的状况;记录两活塞C之间的距离为h.
e.根据数据h列出公式,计算空气中氧气的体积分数.(注:A容器内的固态物质、惰性电热板、活塞部分所占体积忽略不计,活塞与玻璃容器之间的摩擦力也忽略不计)
(1)检查装置气密性的方法是分别移动两活塞C到左右两边刻度为10 cm处,塞紧橡皮塞B,双手将两活塞C向里推,使活塞之间的距离缩小,然后松手,活塞向外移动,直到两活塞C的距离为________cm时停止移动,说明装置气密性好.
(2)b~d的实验步骤中两活塞之间的距离h具体变化情况是________.
(3)空气中氧气的体积分数的计算公式(含字母h)为________.
(4)如果在操作d中惰性电热板没有冷却到原来温度,则e操作中计算出的实验结果比理论值偏________(“大”或“小”).
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学课外兴趣小组,开展了以下两项活动:
某化学课外兴趣小组,开展了以下两项活动: 实验过程中溶液的pH变化曲线如右图所示:
实验过程中溶液的pH变化曲线如右图所示:查看答案和解析>>
科目:初中化学 来源:2011年四川省成都市中考化学模拟试卷(解析版) 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com