
科目:初中化学 来源: 题型:阅读理解
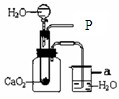 (2009?泉港区质检)周末,小萌与爸爸经过一鱼塘边,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡.经咨询得知,这种固体俗称“鱼浮灵”,主要成分是过氧化钙(CaO2).
(2009?泉港区质检)周末,小萌与爸爸经过一鱼塘边,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡.经咨询得知,这种固体俗称“鱼浮灵”,主要成分是过氧化钙(CaO2).| 实验步骤 | 可能出现的现象 | 解释与结论 |
| 取反应后试管中的上层清液,加入 碳酸钠 碳酸钠 |
澄清石灰水变浑浊 澄清石灰水变浑浊 |
写出有关反应化学方程式(或解释出现现象的原因): Ca(OH)2+Na2CO3═CaCO3↓+2NaOH Ca(OH)2+Na2CO3═CaCO3↓+2NaOH 则CaO2与H2O反应,所得含钙产物中含有 OH- OH- (填阴离子的符号),即有Ca(OH)2生成. |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:新人教版九年级下册《第11章 盐 化肥》2013年单元检测训练卷D(一)(解析版) 题型:填空题
查看答案和解析>>
科目:初中化学 来源:《7.4 酸、碱、盐的应用》2010年同步练习(6)(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com