
分析 (1)根据达菲的化学式可知,该化合物中碳、氢两种元素的质量比为:(碳的相对原子质量×碳原子个数);(氢的相对原子质量×氢原子个数);
(2)该化合物中氧元素的质量分数=$\frac{氧的相对原子质量×氧原子个数}{达菲的相对分子质量}$×100%.
解答 解:(1)根据达菲的化学式可知,该化合物中碳、氢两种元素的质量比为:(12×16):(1×31)=192:31;
(2)该化合物中氧元素的质量分数=$\frac{16×8}{410}$×100%≈31.2%.
故答案为:(1)192:31;(2)31.2%.
点评 本题主要考查学生运用化学式进行计算的能力.解答时要注意解题格式.


 天天向上口算本系列答案
天天向上口算本系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
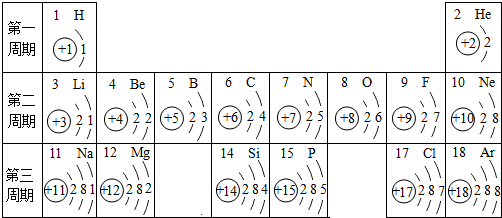
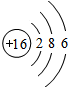 ,它属于非金属(填“金属”与“非金属”)元素;化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子,该离子符号是S2-.
,它属于非金属(填“金属”与“非金属”)元素;化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子,该离子符号是S2-.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 均一、稳定的液体都是溶液 | B. | 溶液都是无色透明的 | ||
| C. | 饱和溶液不能再溶解任何物质 | D. | 浓溶液不一定是饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该混合物可能是Zn、A1,w可能是0.2g | |
| B. | 该混合物可能是Zn、Fe,w可能是0.2g | |
| C. | 若混合物为Zn、Cu,w是0.1g,则该混合物中锌的质量分数为50% | |
| D. | 若混合物为Zn、Mg,w是0.1g,则该混合物中锌的质量分数为50% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com