
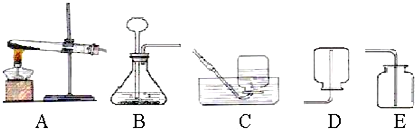
分析 (1)根据反应物的状态和反应条件确定实验室制取氧气的发生装置;根据氧气的密度和溶解性选择收集方法;根据二氧化锰的特点回答其作用;根据反应的原理写出反应的方程式;
(2)根据实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳; 二氧化碳能够溶于水,密度比空气大,能使澄清石灰水变浑浊解答;
解答 解:(1)实验室用加热氯酸钾和二氧化锰的混合物制取装置的特征属于固固加热型的A装置,因为氧气的密度比空气大,不易溶于水,故可以采用向上排空气法或排水法收集;其中二氧化锰作为催化剂,起到催化作用;反应的方程式为:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;若用高锰酸钾制氧气,可选A装置,为了防止高锰酸钾小晶粒进入导管,常在试管口放一团棉花,该反应可用化学方程式表示为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
答案:A;催化;2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;一团棉花;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)实验室制取二氧化碳气体,使用的药品是大理石或石灰石和稀盐酸,属于固液常温型,故选B;由于二氧化碳密度比空气密度大;故选择向上排空气法收集;二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
答案:B;密度比空气密度大;CaCO3+2HCl=CaCl2+H2O+CO2↑;Ca(OH)2+CO2═CaCO3↓+H2O.
点评 本题考查了氧气机氢气的制取、收集和反应原理;关键是明确发生装置和收集装置收集的依据.


科目:初中化学 来源: 题型:选择题
| A. | H2在空气中燃烧的火焰为淡蓝色 | |
| B. | 利用H2的还原性可以进行金属冶炼 | |
| C. | 氢气是一种新能源 | |
| D. | 收集满氢气的集气瓶应正放在桌子上 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 食物 | 苹果 | 葡萄 | 牛奶 | 玉米粥 |
| pH | 2.9~3.3 | 3.5~4.5 | 6.3~6.6 | 6.8~8.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
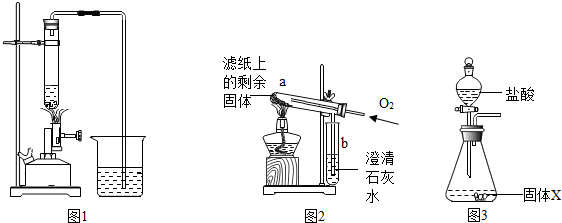
| 步骤 | 操作 | 主要现象 | 结论 |
| Ⅰ | 取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引. | 部分固体被吸引到磁铁上 | 可能有Fe或Fe3O4 |
| Ⅱ | 取滤纸上的剩余固体少量,放入图2所示的试管a中,通入氧气,用酒精灯加热. | 固体剧烈燃烧,b中溶液变浑浊 | 一定有C |
| Ⅲ | 另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸. | 无明显现象 | 一定没有FeO和Fe2O3 |
| Ⅳ | 取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸. | 产生气泡. | 一定有Fe |
| Ⅴ | 在步骤IV所得溶液中逐滴加入KSCN溶液. | 溶液不变红色 | 一定没有Fe3O4 |
| 步骤 | 操作 | 数据 |
| Ⅰ | 重新取部分冷却至室温的固体X,称量其质量为m1. | m1=17.9g |
| Ⅱ | 将称量好的固体X全部放入图3所示的锥形瓶中,称量整套装置及药品的质量为m2;打开分液漏斗旋塞,放入足量稀盐酸后关闭旋塞,待没有气泡产生并恢复至室温,再次称量整套装置及药品的质量为m3. | m2=317.9g m3=317.3.g |
| Ⅲ | 将锥形瓶中剩余的固体过滤、洗涤并干燥,称量其质量为m4. | m4=1.1g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化学技术可以提高人类的生活质量 | B. | 化学工业一定会污染环境 | ||
| C. | 自然界中的现象与化学学科无关 | D. | 生活中不需要懂得化学知识 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Z Y X | B. | Y X Z | C. | X Y Z | D. | X Z Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com