
(10分)某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制200g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为 g,水的体积为 mL
(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后 (按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是 .
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)下图表示用上述配制的氢氧化钠溶液与20 g某稀盐酸发生反应后溶液温度的变化情况。

①根据曲线判断,当加入氢氧化钠溶液的质量为 时,反应恰好完全进行。
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为 (写化学式)。
③试计算该稀盐酸中溶质的质量分数(请写出计算过程)
科目:初中化学 来源: 题型:
(10分)
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究。
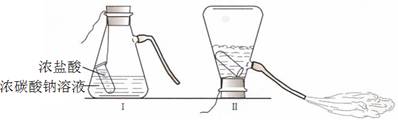
【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想(二):废液中的溶质只有NaCl。
猜想(三):废液中的溶质是NaCl和HCl。
猜想(四):废液中的溶质是__________________。
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的。他的理由是___________________
____________________________________________。
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想(二)正确。小强的实验____________(填“能”或“不能”)验证猜想(二)的正确性,原因是________________。
(2)小丽为验证猜想(三),选用大理石做试剂。若猜想(三)是正确的,验证时反应的化学方程式为____________________________________。
(3)若验证猜想(四)是否正确,下列试剂中可选用的有____________(填序号)。
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行_______________操作即可从废液中得到NaCl固体。此方法的缺点是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0 g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | 0.3g |
查看答案和解析>>
科目:初中化学 来源:2012届山东省东营济军生产基地实验学校九年级上学期阶段检测化学试卷(带解析) 题型:计算题
(10分)某化学兴趣小组为测定大理石中碳酸钙的含量,将过量的稀盐酸加入到20 g大理石中(其它成分不与盐酸反应),把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
| 时间/s | O | 20 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | O | 3.O | 5.O | 6.O | 6.6 | 6.6 | 6.6 |

查看答案和解析>>
科目:初中化学 来源:2011-2012学年山东省九年级上学期阶段检测化学试卷(解析版) 题型:计算题
(10分)某化学兴趣小组为测定大理石中碳酸钙的含量,将过量的稀盐酸加入到20 g大理石中(其它成分不与盐酸反应),把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
|
时间/s |
O |
20 |
40 |
60 |
80 |
100 |
120 |
|
增加的质量/g |
O |
3.O |
5.O |
6.O |
6.6 |
6.6 |
6.6 |
试回答下列问题:
(1)请在右边的坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;

(2)从表中可以看出,20 g大理石样品与盐酸反应生成的CO2质量最多是 g;
(3)计算大理石样品中碳酸钙的质量分数。
查看答案和解析>>
科目:初中化学 来源:2011-2012学年山东东营济军生产基地实验学校九年级上学期阶段检测化学试卷(解析版) 题型:计算题
(10分)某化学兴趣小组为测定大理石中碳酸钙的含量,将过量的稀盐酸加入到20 g大理石中(其它成分不与盐酸反应),把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
|
时间/s |
O |
20 |
40 |
60 |
80 |
100 |
120 |
|
增加的质量/g |
O |
3.O |
5.O |
6.O |
6.6 |
6.6 |
6.6 |
试回答下列问题:
(1)请在右边的坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;

(2)从表中可以看出,20 g大理石样品与盐酸反应生成的CO2质量最多是 g;
(3)计算大理石样品中碳酸钙的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com