
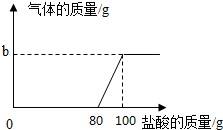
 在实验室中,化学兴趣小组的同学发现了一瓶敞口的氢氧化钠固体.他们对该固体的成分进行了定量实验分析:称取固体21.3克放入锥形瓶中,加入一定量的水配制成50克溶液,再向锥形瓶中依次滴加20克盐酸充分反应.测得部分数据与图象如表.请根据有关信息回答问题.
在实验室中,化学兴趣小组的同学发现了一瓶敞口的氢氧化钠固体.他们对该固体的成分进行了定量实验分析:称取固体21.3克放入锥形瓶中,加入一定量的水配制成50克溶液,再向锥形瓶中依次滴加20克盐酸充分反应.测得部分数据与图象如表.请根据有关信息回答问题. | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量 | 20 | 20 | 20 | 20 | 20 | 20 |
| 锥形瓶中物质的质量 | 70 | 90 | a | 130 | 147.8 | 167.8 |
分析 (1)根据前四次加入盐酸后溶液中增加的质量是:130g-50g=80g,所以每次增加的都是加入盐酸的质量,所以a的数值为110,依据质量守恒定律计算生成二氧化碳的质量;
(2)根据氢氧化钠易与空气的中二氧化碳反应生成了碳酸钠,碳酸钠与盐酸反应生成二氧化碳气体,可判断氢氧化钠是否变质;
(3)根据碳酸钠与盐酸的反应,由二氧化碳的求出碳酸钠的质量,即可求出氢氧化钠的质量分数.
解答 解:(1)敞口放置的氢氧化钠固定会部分和空气中的二氧化碳反应生成碳酸钠,当加入稀盐酸时,HCl先和NaOH反应,后和Na2CO3反应.
由表中的数据可知,第1、2、4次加入盐酸的质量就等于锥形瓶中增加的质量,所以第3次加入盐酸后物质的质量就是2次锥形瓶中物质的质量再加上盐酸的质量,故a的值为:90g+20g=110g,由表中的数据可知,第6次加入盐酸的质量就等于锥形瓶增加的质量,说明了第5次加入的盐酸已将碳酸钠完全反应,则生成的二氧化碳的质量:120g+50g-167.8g=2.2g;
(2)得出该试剂已部分变质的结论,其依据是:滴加盐酸至80g时,开始时有二氧化碳生成,证明有碳酸钠存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钠反应,从而证明氢氧化钠存在;
(3)设固体中碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{x}$=$\frac{44}{2.2g}$
x=5.3g
所以该固体中氢氧化钠的质量是21.3g-5.3g=16g.
故答案为:(1)110,2.2;
(2)滴加盐酸至80g时,开始时有二氧化碳生成,证明有碳酸钠存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钠反应,从而证明氢氧化钠存在;
(3)16g.
点评 根据数据列表或关系图,找出反应中某物质的质量是这一类问题的解决方法.


科目:初中化学 来源: 题型:选择题
| A. | 石油分解后可得到汽油、煤油、柴油等一系列产品 | |
| B. | 把煤加工成蜂窝煤可使之燃烧更加充分 | |
| C. | 天然气是比煤、石油更加清洁的化石燃料 | |
| D. | 汽油中加入适量的乙醇可减少汽车尾气的污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰 | |
| B. | 在空气中打开盛浓盐酸的试剂瓶瓶塞,产生白雾 | |
| C. | 二氧化碳通入氯化钙溶液中产生白色沉淀 | |
| D. | 将氢氧化钠溶液滴入硫酸铜溶液中,产生蓝色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 出行方式尽量采用步行、骑自行车或乘公交车 | |
| B. | 推广无纸化办公,使用再生纸且双面打印 | |
| C. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| D. | 用剧毒农药杀灭韭菜根部的害虫 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1.5g | B. | 1.3g | C. | 2.0g | D. | 1.2g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
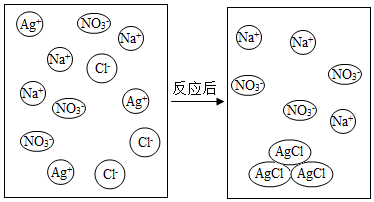 如图是氯化钠溶液和硝酸银溶液反应的示意图.
如图是氯化钠溶液和硝酸银溶液反应的示意图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com