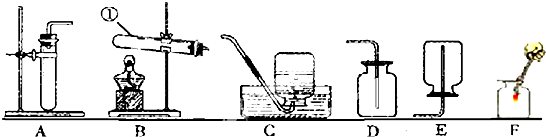
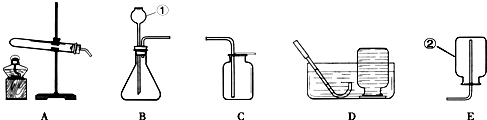
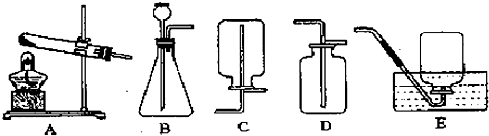
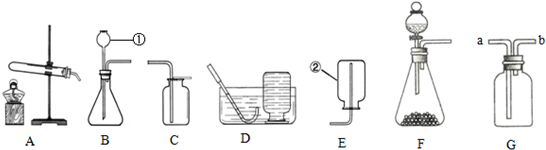
解:(1)仪器的名称为:①长颈漏斗;②集气瓶.
(2)氯酸钾是固体,反应条件是加热,发生装置应选A,氧气不易溶于水,可用排水法收集,密度比空气大,可用向上排空气法收集,故应选择的装置组合是A、C(或D);单独加热氯酸钾反应速度太慢,因此加入二氧化锰作反应的 催化剂.反应的化学方程式为 2KClO
3
2KCl+3O
2 ↑
.
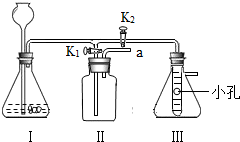
(3)检查装置B的气密性的方法是 关闭止水夹,从长颈漏斗内加水至漏斗内有水,看液面是否下降,若不下降,则气密性良好..
(4)氢气密度比空气小,气体应从b管进,将空气从a管排出.
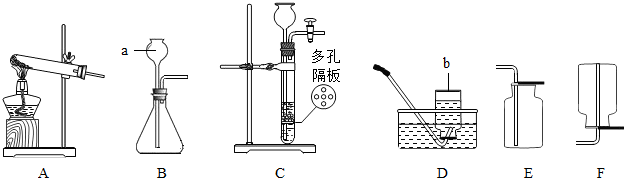
(5)电石是固体,水是液体,发生装置选择B,乙炔密度比空气略小,不能用排空气法收集,不溶于水,可用排水法收集.故收集装置选择D;电石与水反应生成乙炔和氢氧化钙,化学方程式为CaC
2+2H
2O=C
2H
2↑+Ca(OH)
2故答案为:(1)①长颈漏斗;②集气瓶.
(2)AC或AD 催化剂. 2KClO
3
2KCl+3O
2 ↑.
(3)关闭止水夹,从长颈漏斗内加水至漏斗内有水,看液面是否下降,若不下降,则气密性良好..
(4)b
(5)B; D. CaC
2+2H
2O=C
2H
2↑+Ca(OH)
2分析:(1)直接写仪器名称;
(2)根据氯酸钾分解制氧气的原理、装置分析
(3)根据装置气密性检查的方法分析
(4)根据氢气的密度分析
(5)根据发生装置和收集装置选择依据分析
点评:了解气体制取装置的选择和连接方法;掌握氧气的制取装置、原理和检验方法;能够根据所给物质的性质来选择发生和收集装置

 2KCl+3O2 ↑
2KCl+3O2 ↑ 2KCl+3O2 ↑.
2KCl+3O2 ↑.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案