
 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
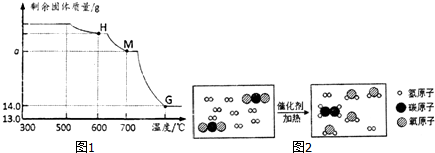
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO | B. | NO | C. | CO2 | D. | SO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 莽草酸中氧元素质量分数最大 | |
| B. | 一个“达菲”分子中含有60个原子 | |
| C. | 莽草酸分子中C、H、O三种元素的原子个数比为7:10:5 | |
| D. | 莽草酸的相对分子质量是l74 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 若要除去H2中的CO2,可在此装置中装入NaOH溶液,气体从B端通入 | |
| B. | 若用排空法往装置内收集H2时,气体应从A端通入 | |
| C. | 若用水将此装置中的空气排出,水应从A端进入 | |
| D. | 若用排水法往装置内收集CO时,气体应从A端通入 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com