
【题目】如图为甲、乙两种固体的溶解度曲线。下列说法正确的是(_____)

A甲物质的溶解度比乙大
B将接近饱和的甲溶液变为饱和溶液,可采用蒸发溶剂或降温的方法
Ct1°C时,甲、乙两种物质的饱和溶液中,溶质质量分数均为15%
Dt2°C时,将20g甲物质放入50g水中,所得溶液的质量为______________g
科目:初中化学 来源: 题型:
【题目】实验室制取 CO2,并验证 CO2 和 CO 的性质的式样(如下图所示),请回答问题:
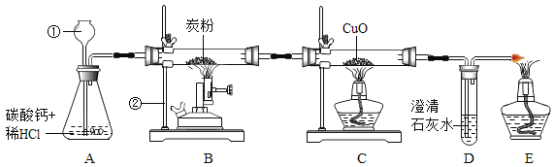
Ⅰ.写出标有序号的仪器名称①______②_____
Ⅱ. 能证明 CO 具有还原性的实验现象为_____,化学方程式为_____; E 处放一点燃的酒精灯的目的是_____
Ⅲ.写出 A 中反应的化学方程式_____,实验结束时,先停止 B、C 处的加热,继续通一会A 中产生的气体,其目的是_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,万物之基,是人类宝贵的自然资源,我们每个人都要爱护和节约。
①A中小卵石和石英砂的作用是_____。
②在宏观、微观、符号之间建立联系是化学特有的思维。根据电解水实验,回答下列问题。

从宏观上观察:如图B所示,试管甲和乙中产生气体的体积比约为_____;从符号上表示:电解水的化学方程式为_____;反应的基本类型是_____。从微观上下列说法正确的是_____(填字母)。
A 水是由氢原子和氧原子构成的
B 水是由氢分子和氧原子构成的
C 每个水分子是由2个氢原子和1个氧原子构成的
D 水是由水分子构成的
③在如图C的空白处画出反应的微观过程_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体质量/g | 8.4 | 6.8 | 5.2 | 3.6 | 3.6 |
请认真分析表中的数据,回答下列问题:
(1)表示样品与稀硫酸恰好完全反应的是上表中第________次操作;
(2)计算样品中锌的质量分数; ____
(3)计算实验中所用稀硫酸的溶质质量分数。 ______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种物质(不含结晶水)的溶解度曲线.下列说法中正确的是

A.甲的溶解度大于乙的溶解度
B.t1℃时,50g甲的饱和溶液中有15g甲
C.t2℃时甲的饱和溶液降温至t1℃变为不饱和溶液
D.当甲中含有少量乙时,可以用降温结晶的方法提纯甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如下图所示。
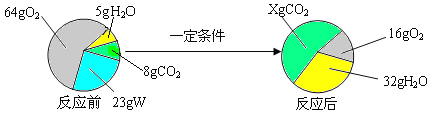
下列关于以上反应的说法中,正确的是
A. X的值为44 B. W由碳、氢两种元素组成
C. 该反应属于置换反应 D. W中碳、氢元素质量比为4∶1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组通过探究活动学习化学知识,请你一起参与探究性学习,并回答有关问题。
探究主题:水溶液中发生复分解反应的实质。
相关信息:一定体积的溶液中,离子的数目越多,其浓度越大。电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小。相同温度下同种溶液电导率越大,离子浓度越大。
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2~3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示。
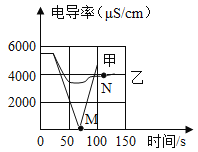
①写出反应的化学方程式:_______________。
②甲曲线M点时混合液体呈____________色。
③通过对甲曲线的分析,下列说法正确的是___________(填字母)。
A、M点前曲线下滑的过程中,H+和OH-结合成H2O,Ba2+和SO42-结合成BaSO4
B、M点时离子浓度几乎为零
C、M点后溶液电导率逐渐增大,仅由于溶液中H+数目在逐渐增大
(3)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2~3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如图乙曲线所示。
①通过对乙曲线的分析,下列说法错误的是___________(填字母)。
A、开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B、电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C、整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是_______________(填离子符号)。
③该实验中实际参加反应的离子是____________________。
实验结论:通过分析可知,溶液中发生复分解反应的实质是参与反应的离子结合生成了难电离的____________,导致溶液中的离子浓度_________(填“增大”或“减小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
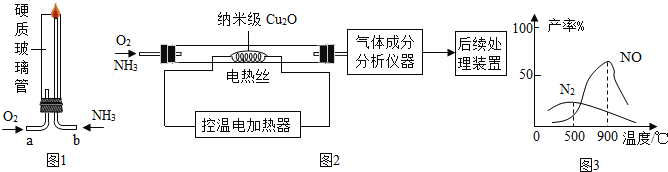
【题目】某化学兴趣小组为了探究NH3在不同环境下与O2的反应,进行图1和图2两组实验,同学们根据图2实验中气体成分分析数据,绘制了如图3的曲线图。
(查阅资料)
①氨气是一种有刺激性气味的气体,在高浓度氧气中才能燃烧,生成氮气和水;
②在纳米级Cu2O的催化作用下,氨气与氧气在不同的温度下发生以下不同的化学反应(表达式中条件已省略): 4NH3+5O2═4NO+6H2O ,4NH3+3O2═2N2+6H2O;工业上用NO制备硝酸、氮肥等化工产品。
请根据所给信息回答:
(1)图1实验过程中,要先通__________一段时间,再通入另一种气体并点燃,可以避免空气污染。
(2)氨气在高浓度氧气中燃烧的化学方程式为___________________________________。
(3)图2实验中,若后续处理装置是为工业制备硝酸提供NO,根据图3分析,最好将电热丝的温度控制在__________℃左右。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com