
| 12b |
| 44 |
| 3bm |
| 11 |
| 3bm |
| 11 |
| 11m-3bm |
| 11 |
| ||
| m |
| 11m-3b |
| 11m |


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
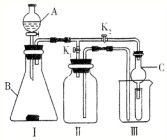 某校化学兴趣小组设计的实验装置如图所示,既可用于制取气体,又可用于验证物质性质.
某校化学兴趣小组设计的实验装置如图所示,既可用于制取气体,又可用于验证物质性质.查看答案和解析>>
科目:初中化学 来源:2012届湖北省黄冈市中考模拟化学试卷(B卷)(带解析) 题型:推断题
某校化学兴趣小组设计的实验装置如图所示,既可用于制取气体,又可用于验证物质性质。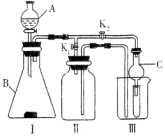
①写出仪器的名称:A____________;B____________。
②当打开K1、关闭K2时,利用Ⅰ、Ⅱ装置可直接进行的实验是_______(填序号)。
a. 大理石与稀盐酸反应制取二氧化碳
b. 锌与稀硫酸反应制取氢气
③某同学当打开K2、关闭K1时,利用Ⅰ、Ⅱ装置可验证二氧化碳与水反应生成了碳酸,此时试管中盛放的物质是_____________,可观察到的现象是__________________(C为干燥管,用于防止液体倒吸)。
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省吴江市九年级5月教学调研测试化学试卷(解析版) 题型:选择题
某校化学兴趣小组设计用下图所示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。[查阅资料]:①Fe与浓H2SO4反应,加热,有SO2生成;②C与浓H2SO4反应,加热,有CO2和SO2生成;③SO2可使澄清石灰水变浑浊;④SO2可使品红溶液的红色褪去,而CO2不能;⑤SO2可与酸性KMnO4溶液反应使其褪色,而CO2不能;⑥碱石灰的主要成分为NaOH和CaO。
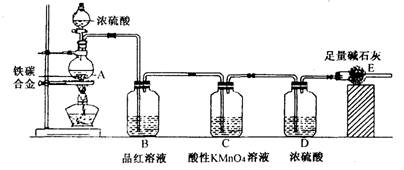
[实验探究]称取mg铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg。下列对实验结果分析正确的是
A.B装置作用是为了除去反应中生成的SO2
B.依据实验数据计算得出铁的质量分数为(3b-11m)/11m
C.装置内的CO2难以赶尽,E质量偏小,导致铁的质量分数偏小
D.SO2未被酸性KMnO4除尽也可能会引起铁的质量分数偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com