
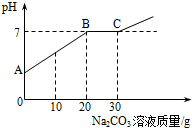
 向21.88g含有少量CaCl2的稀盐酸中逐渐滴加10.6%的Na2CO3溶液,加入Na2CO3溶液的质量和溶液pH的关系如图所示.请回答下列问题:
向21.88g含有少量CaCl2的稀盐酸中逐渐滴加10.6%的Na2CO3溶液,加入Na2CO3溶液的质量和溶液pH的关系如图所示.请回答下列问题:分析 根据加入碳酸钠溶液时,碳酸钠先和稀盐酸反应生成氯化钠、水和二氧化碳,至加入20g碳酸钠溶液时与稀盐酸恰好完全反应;继续加入碳酸钠溶液时,碳酸钠与氯化钙反应碳酸钙沉淀和氯化钠,至加入30g碳酸钠溶液时与氯化钙恰好完全反应;根据提供的数据可以计算生成气体的质量,生成沉淀的质量,加入30g碳酸钠溶液充分反应后所得溶液中溶质的质量分数.
解答 解:图中B→C段表示发生的反应是碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl;
(2)(2)设生成二氧化碳气体的质量为x,生成氯化钠的质量为m,生成沉淀碳酸钙的质量为y,生成氯化钠的质量为n,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 117 44 106 100 117
20g×10.6% m x (30g-20g)×10.6% y n
$\frac{106}{20g×10.6%}$=$\frac{117}{m}$=$\frac{44}{x}$
$\frac{106}{(30g-20g)}$=$\frac{100}{y}$=$\frac{117}{n}$
x=0.88g,y=1g,m=2.34g,n=1.17g,
(3)加入30g碳酸钠溶液充分反应后所得溶液中溶质的质量分数为:$\frac{2.34g+1.17g}{21.88g+30g-0.88g-1g}$×100%=7.02%.
答:加入30g碳酸钠溶液充分反应后所得溶液中溶质的质量分数为7.02%.
故答案为:(1)CaCl2+Na2CO3=CaCO3↓+2NaCl;
(2)0.88,1;
(3)7.02%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 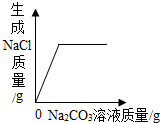 表示向一定质量的盐酸和氯化钙的混合溶液中逐滴加入碳酸钠溶液至过量 | |
| B. | 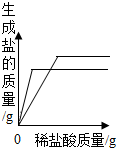 表示向等质量的镁和锌中分别滴加稀盐酸至过量 | |
| C. | 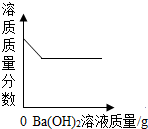 表示向一定质量的稀硫酸中逐滴加入氢氧化钡溶液至过量 | |
| D. | 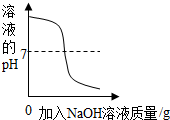 表示向一定体积的稀盐酸中逐滴加入氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生活中不用含碳的物质 | B. | 较低的二氧化碳排放 | ||
| C. | 停止含碳矿物的开采和加工 | D. | 禁止使用煤炭、石油 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐溶液不一定呈中性 | |
| B. | 碱的组成中一定含有“OH”原子团 | |
| C. | 物质溶于水时一定伴随着吸热和放热两个过程 | |
| D. | 中和反应的实质是H+离子与OH-离子反应生成H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com