
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)工业上生产尿素[ CO(NH2 )2 ] 的反应微观示意图如下:
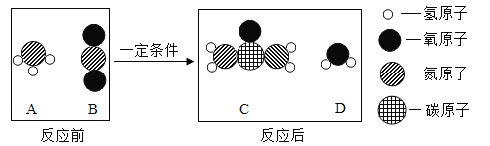
①从微观角度看,上图中四种物质都是由__________构成;
②从宏观的角度看,上图四种物质中属于氧化物的有_____________ ( 填字母序号);
③写出工业上生产尿素的化学方程式_____________。
(2)下表是元素周期表中第2、3周期的元素,请回答有关问题。
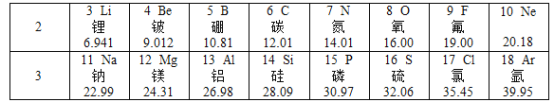
①下列各组具有相似化学性质的元素是________(填字母序号);
ANa、Cl BO、S CF、C1 DCl、Ar
②写出一条第三周期元素原子的核外电子排布规律___________;
③第7号元素与第12号元素的原子形成化合物的化学式为_________;
④某粒子的结构示意图为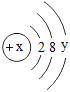 当x-y=8时,该粒子的符号为__________;
当x-y=8时,该粒子的符号为__________;
⑤具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是________(填字母序号)。
ANO和O2 BCO和 N2 CSO2和 CO2 DPO43-和SO42-
【答案】分子 BD 2NH3+CO2 CO(NH2)2+H2O BC 同一周期的元素的原子,核外电子层数相同 Mg3N2 S2- BD
CO(NH2)2+H2O BC 同一周期的元素的原子,核外电子层数相同 Mg3N2 S2- BD
【解析】
(1)①由物质的微观构成可知,图中四种物质都是由分子构成;故填:分子;
②据图可以看出,B表示的是二氧化碳,D表示的是水,二氧化碳和水属于氧化物。故填:BD;
③据图可以看出,A是氨气,B是二氧化碳,C是尿素,D是水,所以工业上生产尿素的化学方程式是:2NH3+CO2 CO(NH2)2+H2O。故填:2NH3+CO2
CO(NH2)2+H2O。故填:2NH3+CO2 CO(NH2)2+H2O。
CO(NH2)2+H2O。
(2)①具有相似化学性质的元素则最外层电子数相同,在元素周期表中位于同一族;
A.Na和Cl不是同一族,不具有相似的化学性质,故错误;
B.O和S是同一族,具有相似的化学性质,故正确;
C.F和Cl是同一族,具有相似的化学性质,故正确;
D.Cl和Ar不是同一族,不具有相似的化学性质,故错误;
故填:BC;
②第三周期元素原子的核外电子排布规律:由左至右最外层电子数依次递增或核外电子层数都是3层。故填:由左至右最外层电子数依次递增;
③第7号元素与第12号元素的原子形成化合物是氮化镁,氮化镁中镁元素化合价显+2,氮元素化合价显-3,根据化合物中元素化合价代数和为零可知,氮化镁的化学式是Mg3N2。故填:Mg3N2;
④某粒子的结构示意图为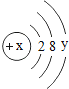 ,x-y=8,即y=x-8;由此可以看出核外电子数为2+8+(x-8)=x+2,核外电子数比核内质子数多2,则依据形成离子的特点,故x=16,y=8,该粒子为硫离子,符号为S2-。故填:S2-;
,x-y=8,即y=x-8;由此可以看出核外电子数为2+8+(x-8)=x+2,核外电子数比核内质子数多2,则依据形成离子的特点,故x=16,y=8,该粒子为硫离子,符号为S2-。故填:S2-;
⑤根据原子序数=质子数=核外电子数。
A、氧原子的核外电子数为8,氮原子的核外电子数为7,所以一氧化氮和氧气的电子数分别是15和16,不属于等电子体;
B、碳、氮、氧原子的核外电子数分别为6、7、8,由于一氧化碳和氮气的原子个数都为2,核外电子个数都为14,属于等电子体;
C、碳、氧、硫原子的核外电子数分别为6、8、16,所以二氧化硫和二氧化碳的电子数分别是32和22,不属于等电子体;
D、氧、磷、硫原子的核外电子数分别为8、15、16,磷酸根(PO43-)和和硫酸根(SO42-)的原子个数都为5,磷酸根带三个单位负电荷,其的核外电子数为15+16×4+3=82个,硫酸根带两个单位负电荷,其的核外电子数为16+16×4+2=82个,电子个数相等,属于等电子体。
故选:BD。


科目:初中化学 来源: 题型:
【题目】《关于汞的水俣公约》旨在控制和减少全球汞排放。下列有关汞的说法不正确的是( )

A.汞俗称水银,常温呈液态,属于物理性质
B.保持汞化学性质的最小粒子是汞原子
C.实验室通风口装在下方,降低汞蒸气浓度
D.据上图,汞的相对原子质量是200.6g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,是人类最宝贵的自然资源,爱惜水、保护水是每个公民的义务和责任。
(1)下列说法错误的是_______________(填序号)
①农业和园林浇灌,改大水漫灌为喷灌、滴灌
②将生活用水、地表雨水分类处理,可减少污染,保护水资源
③淡水资源很丰富,是取之不尽、用之不竭的
(2)生活中常用___________区分硬水和软水,通过_________来降低水的硬度;实 验室中常用_____________的方法除去不溶于水的杂质。
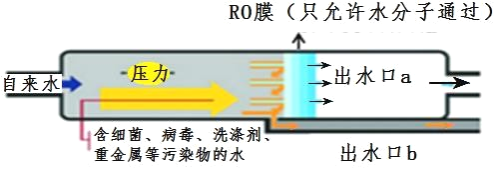
(3)如图显示了家庭净水器工作原理。
①家庭净水器在RO膜之前,常加入含有__________的滤芯,用来吸附水中的一些溶解性的杂质,除去臭味.
②含有杂质少的出水口是__________(填“出水口a”或“出水口b”)。
③净水器产生的废水,进行再利用的建议是 ______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】维持人类生命和健康的六大基本营养素主要有蛋白质、糖类、油脂、维生素、无机盐和水, α-丙氨酸是合成蛋白质的基础物质之一,其分子结构如图所示(注“-”表示原子之间相互 连接),试计算:

(1)α-丙氨酸的相对分子质量为 _____________ ;
(2)α-丙氨酸中碳元素、氢元素、氧元素的质量比为 _____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器内,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法错误的是( )
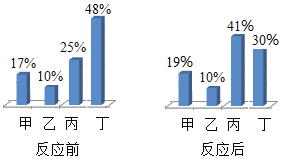
A. 该反应符合质量守恒定律
B. 生成的甲,丙两物质的质量比为8:1
C. 乙可能是该反应的催化剂
D. 参加反应的丁的质量等于生成的甲和丙的质量之和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】初三某化学兴趣小组同学。依据教材实验对化学反应前后质量变化进行了探究。
(查阅资料)碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
(实验装置设计)甲、乙、丙小组同学分别设计如图装置:
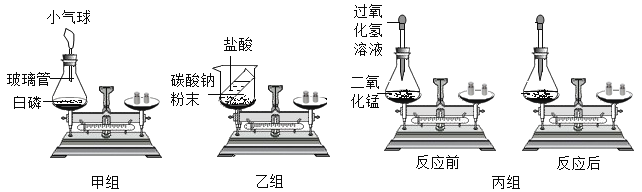
(讨论与探究)(1)甲小组实验中,白磷燃烧时,在锥形瓶底部加入少量水,其目的是:_____。
(2)请根据乙组和丙组设计的“质量守恒定律”的实验装置进行探究,并按要求完成乙组和丙组。
①乙组实验结束后可观察到天平_____(是或否)平衡;此反应_____(填“遵守”或“不遵守”)质量守恒定律。
②丙组过氧化氢溶液分解反应前后各物质质量总和的测定,得出参加化学反应的各物质的质量总和_____(填“大于”、“等于”或“小于”)反应后生成的各物质的质量总和。该反应中二氧化锰起_____作用。
(实验结论)通过甲、乙、丙实验探究,你得到的结论是:_____。
(实验分析)化学反应的过程是_____重新组合的过程,即在一切化学反应中,反应前后原子的_____没有改变,原子的_____没有增减,原子的_____也没有变化,所以化学反应遵守质量守恒定律。
(反思与交流)通过甲、乙、丙小组实验的探究,你得到的启示是:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表为元素周期表中部分元素的相关信息,利用下表回答相关问题。
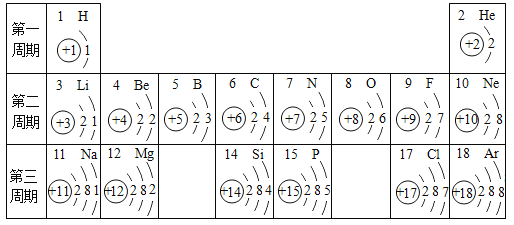
(1)请画出16号元素原子结构示意图__________________,化学反应中该原子比较容易________(选填“得到”或“失去”)电子变成离子。
(2)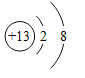 表示的是________(填化学符号)。
表示的是________(填化学符号)。
(3)仔细观察上表,我们能发现很多规律:
①同周期(同一横行)元素的原子核外____________数相同,____________________数从左到右依次递增;
②同族(同一纵行)元素的原子核外____________________数相同,____________数从上到下依次递增。
(4)相对原子质量与原子真实质量之间存在紧密的关系(见下表),根据下表判断6.02×1023个钠原子的质量y为______________。请归纳下表中的规律:6.02×1023个某原子的质量在数值上等于该原子的__________。
碳 | 氧 | 钠 | |
相对原子质量 | 12 | 16 | 23 |
6.02×1023个原子的质量 | 12g | 16g | y |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出符合下列要求的物质(或主要成分)的化学式
(1)相对分子质量最小的氧化物_____;
(2)铅蓄电池中含有的一种酸________;
(3)会造成温室效应的气体单质______;
(4)可以治疗胃酸过多的一种碱_______;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com