
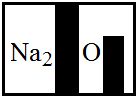 (2012?黄冈)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图所示)的无色溶液,他们对此产生了兴趣.
(2012?黄冈)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图所示)的无色溶液,他们对此产生了兴趣.| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液,静止一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀,后产生大量气泡 |


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
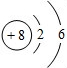 ,从图中你获得的信息有(写二条即可)
,从图中你获得的信息有(写二条即可)
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
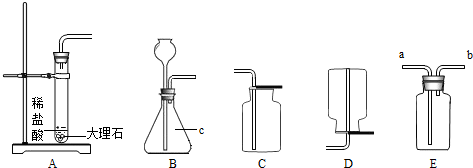
查看答案和解析>>
科目:初中化学 来源:2011年湖北省黄冈市浠水县散花中学中考化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com