

分析 根据质量守恒定律,混合物前后质量之差为生成的二氧化碳的质量,根据二氧化碳的质量可以计算出碳酸钙和氯化钙的质量,再计算出样品中碳酸钙的质量分数B中溶质的质量分数.
解答 解:(1)由质量守恒定律可知,生成CO2的质量为:12.5g+100g-108.1gg=4.4g
(2)设该石灰石样品中CaCO3的质量为x,生成的氯化钙的质量为y,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{4.4g}$ 解得:x=10g y=11.1g
样品中碳酸钙的质量分数是:$\frac{10g}{12.5g}×100%$=80%
(3)B中溶质的质量分数是:$\frac{11.1g}{108.1g-2.5g}×100%$≈10.5%
答:(1)生成二氧化碳的质量是4.4g;
(2)样品中碳酸钙的质量分数是80%;
(3)B中溶质的质量分数是10.5%.
点评 解决本题的关键是根据前后质量之差得出二氧化碳的质量,然后进行计算.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 清洁剂名称 |  洁厕灵 |  彩漂液 |  漂白水 |
| 功 能 | 清除污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 漂除衣物污渍 |
| 有效成分 | HCl | H2O2 | NaClO |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
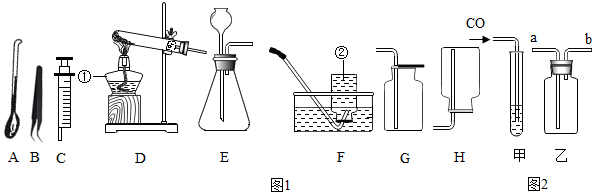
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com