
【题目】金属的性质. 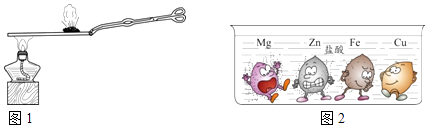
(1)如图1,给铜片左端加热一段时间,铜片右端放置的红磷发生了燃烧,说明铜片具有的性质是 .
(2)如图2,四种金属中活动性最弱的是;选择一种能与盐酸反应的物质,写出反应的化学方程式 .
【答案】
(1)传热性
(2)铜;Zn+2HCl═ZnCl2+H2↑
【解析】解:(1)如图1,给铜片左端加热一段时间,铜片右端放置的红磷发生了燃烧,说明铜片具有的性质是传热性,使白磷的温度达到了着火点.(2)金属与酸反应时金属的活动性越强,反应剧烈,反之亦然,所以从图中可以看出,镁反应最剧烈,其次是锌,然后是铁,不反应的为铜,所以可以判断这四种金属的活动性由强到弱的顺序为:Mg>Zn>Fe>Cu;活动性最弱的是铜,锌与盐酸反应的方程式为Zn+2HCl═ZnCl2+H2↑.所以答案是:(1)传热性;(2)铜,Zn+2HCl═ZnCl2+H2↑.
【考点精析】解答此题的关键在于理解金属的物理性质及用途的相关知识,掌握金属的物理性质: (1)常温下一般为固态(汞为液态),有金属光泽.(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性,以及对金属活动性顺序及其应用的理解,了解在金属活动性顺序里:1、金属的位置越靠前,它的活动性就越强2、位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)3、位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来.(除K、Ca、Na).


科目:初中化学 来源: 题型:
【题目】元素周期表中,钾元素的信息如图所示.下列解释不正确的是( ) 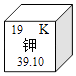
A.原子序数是19
B.原子中核电荷数是19
C.原子中质子数是19
D.相对原子质量是39.10 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类是研究的基本方法。现有几种物质: He 、NaOH 、H2SO4 、NaCl;
以上物质中,可填充飞艇的是_____(写化学式,下同),含有原子团的是_______焰色反应火焰呈黄色的是_______,可除铁锈的是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列矿物的主要成分属于氧化物的是( )
A. 黄铁矿(主要成分为FeS2)
黄铁矿(主要成分为FeS2)
B. 紫晶矿(主要成分为SiO2)
紫晶矿(主要成分为SiO2)
C. 白钨矿 (主要成分为CaWO4)
白钨矿 (主要成分为CaWO4)
D. 黄铜矿(主要成分为CuFeS2)
黄铜矿(主要成分为CuFeS2)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验设计正确的是
A. 用酚酞检验NaOH是否变质 B. 用电解水证明水的组成
C. 用燃烧法除去CO2中的CO D. 用加碘食盐鉴别淀粉和葡萄糖
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用如图所示装置进行实验,研究燃烧的条件. 
已知:白磷的着火点为40℃,红磷的着火点为240℃.
(1)当H2O2溶液与MnO2接触时,发生反应的化学方程式为 .
(2)检查上述装置气密性的实验方案是 .
(3)向Y型管中挤入H2O2溶液后,观察到导管口开始产生气泡时,烧杯中白磷不燃烧;一段时间后,白磷燃烧,此现象能够证明的可燃物燃烧的条件是;若证明可燃物燃烧的另一个条件,依据的现象是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com