
| 项目 | 限值 |
| 色度 | 不超过15度,并不得呈现其他异色 |
| 浑浊度 | 不超过1度,特殊情况下不超过5度 |
| pH | 6.5-8.5 |
| 总硬度(以CaCO3计) | 450mg/L |
| 铝 | 0.2mg/L |
| 铁 | 0.3mg/L |
| 硫酸盐 | 250mg/L |
分析 (1)食品、药品、营养品、矿泉水等物质中的“铁、铝”等不是以单质、分子、原子、离子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(2)根据硬水软化的方法来分析;
(3)根据电解水反应进行分析;
(4)根据化合物中元素正负化合价的代数和为零进行分析;
(5)根据题目信息及化合物中元素质量分数的计算方法分析;
解答 解:(1)食品、药品、营养品、矿泉水等物质中的“铁、铝”等不是以单质、分子、原子、离子等形式存在,这里所指的“铝”是强调存在的元素,与具体形态无关.故填:元素;
(2)加热煮沸能减少水中钙、镁离子的化合物的含量.所以,生活中常用的硬水软化的方法是煮沸;故填:煮沸;
(3)实验室用中将水通电分解,产生氢气和氧气的体积比约为2:1;故填:2:1;
(4)在Ca(ClO)2中,钙为+2价,氧为-2价,设氯元素的化合价为x,则(+2)+2x+(-2)×2=0,x=1;故填:+1价;
(5)由题目信息可知,1L合格的生活饮用水中,CaCO3的质量不能超过450mg,则钙元素的含量应不超过:450mg×$\frac{40}{40+12+16×3}$=180mg;故填:180;
点评 本题考查元素的概念、硬水软化的方法、电解水实验、化合价及元素质量分数的计算等,知识点较多,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 实验室制取气体时,先装药品,再检查装置气密性 | |
| B. | 制作过滤时,现将滤纸放入漏斗内,再用少量水润湿使滤纸紧贴漏斗内壁 | |
| C. | 加热KMnO4并用排水法收集O2,实验结束时熄灭酒精灯,再将导管移出水面 | |
| D. | 稀释浓硫酸时,先在烧杯内倒入浓硫酸,再缓慢注入水中,并不断搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁带燃烧,发出耀眼白光,放出大量热,生成白色固体 | |
| B. | 铁钉与稀盐酸反应,银白色固体逐渐减少至消失,溶液由无色变成浅绿色 | |
| C. | 氢氧化钠溶液与氯化铁溶液混合,产生红褐色沉淀 | |
| D. | 甲烷燃烧产生明亮的蓝色火焰,放热 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


 ”、“○”、“●”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.
”、“○”、“●”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 葡萄糖属于糖类 | |
| B. | 适当提高CO2的浓度有利于植物的光合作用 | |
| C. | 转化过程中涉及三种氧化物 | |
| D. | 无机物和有机物可以相互转化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 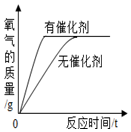 用一定量的双氧水制取氧气 | |
| B. | 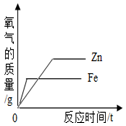 等质量Fe、Zn金属分别与足量等浓度稀硫酸反应 | |
| C. | 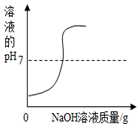 向一定量稀硫酸中逐滴加入氢氧化钠溶液 | |
| D. | 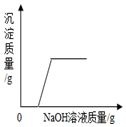 向硝酸铜和硝酸混合溶液中逐滴加入氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
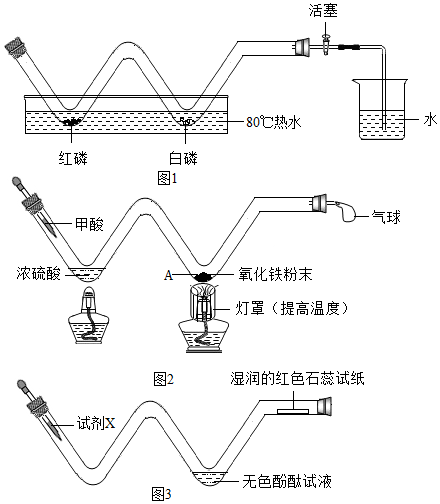
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com