
【题目】(1)我们已经学习了氢氧化钠的性质,知道这种固体要密封保存,原因有:①___________________;②________________。
兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
【对固体猜想】
猜想I:全部是NaOH;猜想II:全部是Na2CO3;猜想III:是NaOH和Na2CO3混合物
【实验和推断】
(2)为进一步确定成分,进行了以下探究:
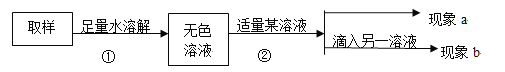
填写以下实验报告:
实验操作 | 实验现象 | 实验结论 |
第一步:用试管取约2mL该无色溶液,滴入适量澄清石灰水。 | 现象a:溶液变浑浊。 | 化学方程式:①___________, 证明有碳酸钠。 |
第二步:静置,取上层清液于另一试管中,滴入无色酚酞溶液。 | 现象b:②__________ | 证明含有NaOH,猜想III成立,是NaOH和Na2CO3混合物 |
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想III成立,理由是:
a、Na2CO3溶液呈碱性; b、__________________________________________________。
(3)兴趣小组按下图实验测定部分变质的NaOH固体中Na2CO3的质量分数。
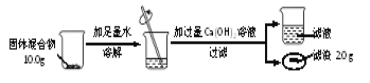
①根据题中信息______(填“能”或“不能”)计算Ca(OH)2溶液的质量分数。
②通过计算,固体混合物中Na2CO3的质量分数是__________________。
【答案】 氢氧化钠固体易潮解 CO2 + 2NaOH = Na2CO3 + H2O或氢氧化钠与空气中二氧化碳反应变质 Na2CO3+Ca(OH)2= 2NaOH+ CaCO3↓ 液体变红 第一步氢氧化钙溶液与碳酸钠溶液反应生成氢氧化钠,干扰第二步氢氧化钠的检验 不能 21.2%
【解析】(1)氢氧化钠固体要密封保存,原因有氢氧化钠固体易吸收空气中的水分,还和空气中的二氧化碳发生反应生成了碳酸钠而变质,故要密封保存;(2)①用试管取约2mL该溶液,滴入适量氢氧化钙溶液,振荡,碳酸钠溶液与氢氧化钙溶液反应生成了碳酸钙沉淀和氢氧化钠,证明有碳酸钠并全部除尽,反应化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;②静置,取上层清液于试管中滴入酚酞溶液,振荡,酚酞变红,说明有氢氧化钠存在,猜想三成立,是NaOH和Na2CO3混合物;③Na2CO3溶液呈碱性,碳酸钠溶液与氢氧化钙溶液反应生成了氢氧化钠,也可以使酚酞变红,不能说明是原溶液中的氢氧化钠还是刚生成的氢氧化钠;为了排除氢氧化钙溶液与碳酸钠溶液反应生成氢氧化钠,干扰第二步氢氧化钠的检验,把第一步中的氢氧化钙溶液换成氯化钙溶液,可达到实验目的。(3) ①由于加入的氢氧化钙溶液质量未知,且本身过量,所以无法求算其质量分数;②设生成2.0g碳酸钙需要的碳酸钠的质量为![]()
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
![]() 2.0g
2.0g
![]()
![]() =2.12g
=2.12g
固体混合物中Na2CO3的质量分数为![]() 。
。
答:(1)根据题中信息不能计算Ca(OH)2溶液的溶质质量分数;(2)固体混合物中Na2CO3的质量分数为21.2%。


科目:初中化学 来源: 题型:
【题目】学习盐的化学性质时,进行了如图所示的实验(提示:氯化钙、氯化钡的溶液都呈中性)

① 碳酸钠是一种重要的盐,甲中碳酸钠溶液中加入酚酞,溶液显______色;乙和丙中都能观察到的实验现象是_______;乙中发生反应的化学方程式是______, 该反应属于_____发应(填基本反应类型);
② 实验结束后,将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并 呈红色;静置,取上层清液于试管中,加入过量氯化钡溶液,有白色沉淀,溶液呈红色。 则废液缸中的废液一定含有指示剂、水、碳酸钙、______; 在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验目的、操作、现象、结论都正确的是
选项 | 实验目的 | 实验操作 | 实验现象 | 实验结论 |
A | 测溶液pH | 用玻璃棒蘸取待测液滴在用蒸馏水润湿的pH试纸上 | 试纸变为浅红色 | 溶液pH为2 |
B | 鉴别NaOH和NH4NO3 | 在装有等量水的试管中分别加入a、b固体 | 加a的试管水温升高,加b的试管水温降低 | a是NaOH b是NH4NO3 |
C | 验证燃烧是否需要O2 |
| 前者不燃烧,后者燃烧 | 燃烧需要O2 |
D | 比较Al、Cu的活泼性 | 将未经打磨的Al条放入CuSO4溶液中 | 无明显现象 | 活泼性Al<Cu |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子。下列说法错误的是()

A. 该反应可能是氧化反应
B. 该图说明化学反应中分子可以再分,原子不能再分
C. 该反应中,参加反应的两种分子个数比为5:1
D. 反应前后,原子的种类与数目都发生了改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从微观视角认识和考察物质世界是学习化学的重要思维方法。
(1)下图是某反应的微观示意图:
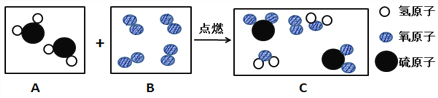
B框中的物质属于________(填序号:①化合物 ②单质 ③纯净物 ④混合物)。此反应化学方程式为____________________。
(2)写出下图A所示的反应化学方程式 _________________ ,属于_____________反应(填反应类型)。该反应前后,溶液减少的离子是 __________。下图B中反应溶液变为无色时,此时溶液中大量存在的粒子是_________________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018 年世界环境日的主题是“人人参与,创建绿色家园”,我们需要:
①清新的空气。绿色植物光合作用产生_______ 气,使人类生生不息;口罩中填充活性炭是利用其_________ 性,以减少污染物的吸入;美丽的霓虹灯中填充的气体是__________。
②洁净的水源。天然水通过蒸发、沙滤、氧化等得到净化,其中蒸发属于_____ 变化(填”物理”或”化学”),自来水生产加入液氯的作用是________。水在通电条件下反应的化学方程式_________, 生成氢气和氧气的体积比是_________ ,0.5mol 水中约含 ________个氢原子。
③清洁的能源。化石燃料煤、石油、甲烷(CH4)中,写出甲烷燃烧的化学方程式_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁是一种活泼金属,除了能与氧气反应,还能与氮气、二氧化碳等反应。为测定镁铝合金(不含其它元素)中镁的质量分数,称量ag镁铝合金粉末,放在如下图所示装置的惰性电热板上,通电使其充分灼烧。下列关于该实验的说法错误的是
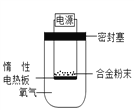
A. 氧气要保证充足
B. 实验结束后一定要再次称量剩余固体质量
C. 用空气代替氧气对实验没有影响
D. 灼烧后的固体为氧化镁和氧化铝的混合物,质量大于ag
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过寻问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:

【进行猜想】
猜想I:原溶液的溶质是NaCl;
猜想II:原溶液的溶质是NaOH;
猜想III:原溶液的溶质是Na2CO3;
猜想IV:原溶液的溶质是NaHCO3。
【查阅资料】
常温下,有关物质的相关信息如下表:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知,原溶液的溶质一定不是NaHCO3,因为_______。
【进行实验】
(1)取少量样品,测得溶液的pH大于7,则原溶液的溶质肯定不是_______。
(2)同学们另取样品又进行了如下实验,实验过程如下:
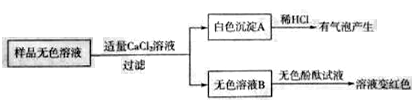
①生成白色沉淀A的化学方程式__________________。
②通过实验可以判断样品无色溶液中含有的溶质有_______
【获得结论】
实验完成后,最终得到的结论:原瓶中的溶质是_____,且已变质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现代循环经济要求综合考虑环境污染和经济效益。高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:提示:(NH4)2CO3溶液呈碱性,40 ℃以上时(NH4)2CO3分解
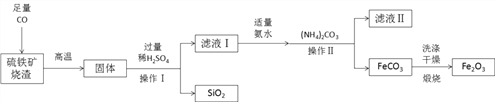
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器有玻璃棒、烧杯、________等。
(2)滤液Ⅰ中主要的溶质是___________________。
(3)加适量氨水的目的是__________________________。
(4)根据题中信息,加入(NH4)2CO3后,该反应必须控制的条件是__________________。
(5)滤液Ⅱ中可回收的产品是_____________(写化学式)。
(6)写出在空气中煅烧FeCO3的化学反应方程式_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com