
| A. | 海水晒盐 | B. | 电池放电 | C. | 冰雪消融 | D. | 干冰升华 |
分析 本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化.
解答 解:A、海水晒盐是水分蒸发过程,没有新物质生成,属于物理变化,故A错;
B、电池放电是由化学能转化为电能,包括了原电池反应原理,其中有新物质生成,属于化学变化,故B正确;
C、冰雪融化是由固态变为液态,只是状态发生了变化,属于物理变化,故C错;
D、干冰升华是由固态直接变为气态,只是状态发生了变化,属于物理变化,故D错.
故选B.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:初中化学 来源: 题型:填空题
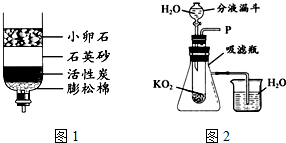 水是最普通、最常见的物质之一.
水是最普通、最常见的物质之一.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ①③⑥ | D. | ②⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
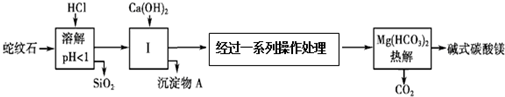
| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | 沉淀不溶 | 沉淀不溶 |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| Mg(OH)2 | 8.6 | 11.1 | 沉淀不溶 | 沉淀不溶 |
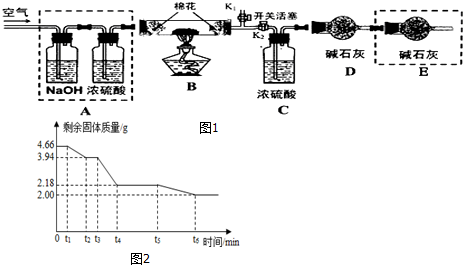
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是A、B、C三种物质的溶解度曲线,请回答:
如图是A、B、C三种物质的溶解度曲线,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
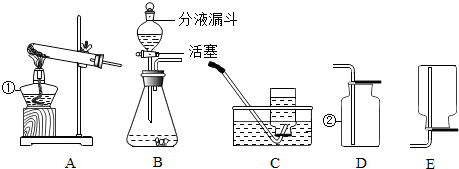
| 烧杯+盐酸 | 大理石 | 充分反应后烧杯+剩余物 | |
| 甲 | 75.0g | 13.2g | 83.8g |
| 乙 | 75.0g | 16.0g | 86.6g |
| 丙 | 95.0g | 13.2g | 103.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某补钙药剂的标签主要内容如图所示,为测定该钙片含量是否符合标注,做如下实验:取10片该钙片粉碎,放人干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的总质量为64.5g.
某补钙药剂的标签主要内容如图所示,为测定该钙片含量是否符合标注,做如下实验:取10片该钙片粉碎,放人干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的总质量为64.5g.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
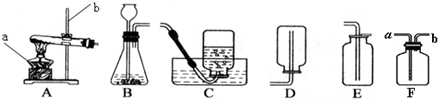
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com