
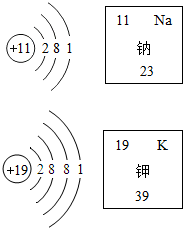
 如图是两种原子的结构示意图和它在元素周期表中的部分信息,完成下列问题.
如图是两种原子的结构示意图和它在元素周期表中的部分信息,完成下列问题.分析 (1)根据钠原子和钾原子质量之比为相对原子质量之比解答;
(2)根据同主族元素从上到下,元素的原子半径逐渐增大解答;
(3)根据钠和水反应生成氢氧化钠和氢气,据此解题.
(4)根据电子在原子中处于不同的能级状态,按能量不同分层排布,即电子在核外是分层排布的解答.
解答 解:(1)钠原子和钾原子质量之比为23:39;
(2)同主族元素从上到下,元素的原子半径逐渐增大;钠原子和钾原子的半径小;
(3)两种原子具有相似化学性质的原因是最外层电子数相同;钠与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑;
(4)电子在原子中处于不同的能级状态,按能量不同分层排布,即电子在核外是分层排布
答案:
(1)23:39;
(2)小;
(3)最外层电子数相同;2Na+2H2O=2NaOH+H2↑;
(4)电子在原子中处于不同的能级状态,按能量不同分层排布,即电子在核外是分层排布.
点评 学生应正确认识原子中电子的排布及微粒的电性,明确原子不显电性,从结构上来理解原子转化为离子的原因


科目:初中化学 来源: 题型:选择题
| A. | 它是有机化合物 | |
| B. | 该化合物中碳、氢、氧、氮四种元素质量比为3:7:2:1 | |
| C. | 它是由碳、氢、氧、氮四种元素组成 | |
| D. | 它的相对分子质量为89 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 66.7% | B. | 75% | C. | 80% | D. | 83.3% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题


查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 加入稀盐酸 的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
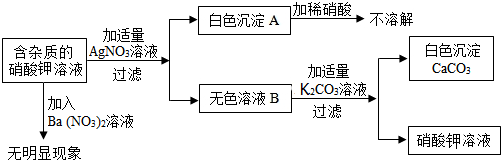
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2:1 | B. | 4:5 | C. | 5:4 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 配制50g5%氯化钠溶液.回答问题:
配制50g5%氯化钠溶液.回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com