
 K2MnO4 +MnO2 +O2↑
K2MnO4 +MnO2 +O2↑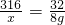
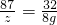
 K2MnO4 +MnO2 +O2↑
K2MnO4 +MnO2 +O2↑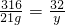


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 实验室制取氧气是初中化学阶段的重要实验.小元同学准确称取7.9g纯净的高锰酸钾加热一段时间后,收集到氧气580mL(标准状况).
实验室制取氧气是初中化学阶段的重要实验.小元同学准确称取7.9g纯净的高锰酸钾加热一段时间后,收集到氧气580mL(标准状况).
| ||
| △ |
| ||
| △ |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:初中化学 来源:《4.3 化学方程式》2013年同步练习(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com