
| 0℃ | 10℃ | 20℃ | 30℃ | |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
| 实验操作 | 实验现象 |
| ①取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液 ②利用装置二进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2 | 没有出现白色沉淀 |
| 实验操作 | 实验现象 |
| ①取100g热开水,加入35g碳酸钠固体,完全溶解,再降温至20℃,取上层清液 ②利用装置一和装置二分别进行实验,连续3分钟向新制得的碳酸钠溶液中通入CO2 | 装置一和装置二中的碳酸钠溶液中均出现白色沉淀 |
分析 (1)由碳酸氢钠和碳酸钠的溶解度变化情况可知,在0℃~30℃,Na2CO3和NaHCO3的溶解度受温度变化影响较大的是碳酸钠;
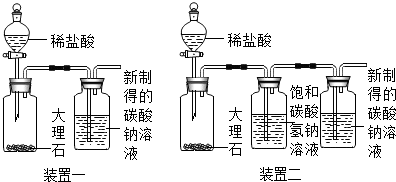
(2)大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)饱和碳酸氢钠溶液能和稀盐酸反应生成氯化钠、水和二氧化碳;
(4)雯雯在最初的实验中没有看到沉淀现象的原因是配制的碳酸钠溶液没有达到饱和;
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是:碳酸氢钠溶解度小于碳酸钠,随着反应的进行,水的质量减小,生成的碳酸氢钠的质量大于反应的碳酸钠;
(6)依据题中信息,可以选择区分碳酸钠和碳酸氢钠的方法.
解答 解:(1)在0℃~30℃,Na2CO3和NaHCO3的溶解度受温度变化影响较大的是碳酸钠.
故填:碳酸钠.
(2)大理石与稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故填:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置二中饱和碳酸氢钠溶液的作用是吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
故填:吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
(4)雯雯在最初的实验中没有看到沉淀现象的原因是配制的碳酸钠溶液没有达到饱和.
故填:配制的碳酸钠溶液没有达到饱和.
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是:碳酸氢钠溶解度小于碳酸钠,随着反应的进行,水的质量减小,生成的碳酸氢钠的质量大于反应的碳酸钠.
(6)区分碳酸钠和碳酸氢钠固体的实验方案是:方法一:取其中一种固体12g,加入100g热开水,充分溶解后,降温至20℃.若有固体析出,为碳酸氢钠,否则为碳酸钠;
方法二:取其中一种固体12g,加入100g20℃的水,充分溶解后,若有白色固体剩余,为碳酸氢钠,否则为碳酸钠.
故填:方法一:取其中一种固体12g,加入100g热开水,充分溶解后,降温至20℃.若有固体析出,为碳酸氢钠,否则为碳酸钠;
方法二:取其中一种固体12g,加入100g20℃的水,充分溶解后,若有白色固体剩余,为碳酸氢钠,否则为碳酸钠.
答案:(1)碳酸钠;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)吸收氯化氢气体,从而排除氯化氢气体对实验的干扰;
(4)配制的碳酸钠溶液没有达到饱和;
(5)碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠
(6)方法一:取其中一种固体12 g,加入100 g热开水,充分溶解后,降温至20℃.若有固体析出,为碳酸氢钠;否则为碳酸钠
方法二:取其中一种固体12 g,加入100 g 20℃的水,充分溶解后,若有白色固体剩余,为碳酸氢钠;否则为碳酸钠
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
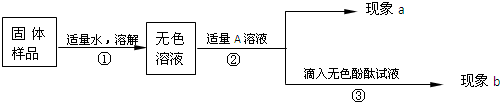
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  液体的倾倒 | B. |  液体的量取 | C. | 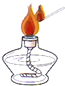 点燃酒精灯 | D. | 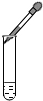 滴加液体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | 二氧化碳 | 一氧化碳 | 氢氧化钠溶液和浓硫酸 | 洗气 |
| B | 硫酸钡 | 碳酸钡 | 足量的稀硫酸 | 溶解、过滤、洗涤、烘干 |
| C | 氯化钙溶液 | 消石灰 | 过量的二氧化碳 | 过滤、蒸发、结晶 |
| D | 氨气 | 水 | 火碱溶液 | 通过盛有火碱溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图为海水淡化装置示意图.
如图为海水淡化装置示意图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com