
金属材料在生产生活中十分广泛
(1)根据下图金属应用实例推断,金属具有的物理性质有_________ (答两点)
(2)生铁和钢都是铁的合金,二者性能不同的原因是_________ ;
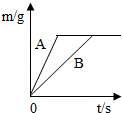
(3)写出工业上以赤铁矿为原料炼铁过程中,一氧化碳与氧化铁发生反应的化学方程式_________ ;
每年因腐蚀而消费掉的金属材料数量惊人,铁生锈的条件是_________ ;防止金属腐蚀是保护金属资源的一条有效途径,保护金属资源的途径还有_________ (答一条即可);
(4)将一定量的锌粉放入稀硫酸、硫酸亚铁、硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加盐酸有气泡产生.则滤渣中一定含有的固体是_________ ;滤液中一定不含的物质是_________ .
(1)导电性、导热性 (2)含碳量不同
(3)3CO+Fe2O3 3CO2+2Fe;与水和氧气同时接触;寻找金属的替代品
3CO2+2Fe;与水和氧气同时接触;寻找金属的替代品
(4)铁、铜;硫酸、硫酸铜
解析试题分析:(1)电缆是利用了金属的导电性,热水壶是利用了金属的导热性,金属丝体现了金属的延展性,故答案为:导电性、导热性
(2)生铁和钢的含碳量不同,生铁的含碳量是2%至4.3%,钢的含碳量是0.03%至2%之间,故答案为:含碳量不同
(3)一氧化碳与氧化铁发生氧化还原反应,生成铁和二氧化碳,反应条件是高温;铁在潮湿的环境容易生锈;寻找金属的替代品、改变金属的内部结构等都是保护金属资源的有效途径.故答案为:3CO+Fe2O3 3CO2+2Fe;与水和氧气同时接触;寻找金属的替代品;
3CO2+2Fe;与水和氧气同时接触;寻找金属的替代品;
(4)根据“在金属活动性顺序里,排在氢前面的金属能与酸反应产生氢气”这一理论,结合题意中的“向滤渣中加盐酸有气泡产生”可以断定“将一定量的锌粉放入稀硫酸、硫酸亚铁、硫酸铜的混合溶液中,充分反应后”一定有铁生成,又因为“在金属活动性顺序里,只有排在前面的金属才能把排在后面的金属从它的盐溶液中置换出来,而且弱的金属先被置换出来”,锌与硫酸亚铁、硫酸铜的混合溶液反应,先置换出铜,所以滤渣中一定含有的固体是铁、铜;液中一定不含的物质是硫酸、硫酸铜.故答案为:铁、铜;硫酸、硫酸铜.
考点:金属的物理性质及用途;金属的化学性质;铁的冶炼;生铁和钢;金属锈蚀的条件及其防护;金属资源的保护.
点评:此题综合性较强,主要考查了金属的物理性质和化学性质,是一道不错的题目.


 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:初中化学 来源: 题型:填空题
整理和归纳是有效的学习方法。下面是某学习小组的同学对Mg、 Fe、Cu、Hg、Ag五种金属相关知识的归纳复习,请你参与并回答问题。
(1)从物理性质上看,每种金属都有自己的特性。你认为Hg与其他四种金属的不同之处是:____________________________________________________。
(2)从化学性质上看,与盐酸反应最剧烈的是,这五种金属中,有一种金属的盐溶液能与其他四种金属发生反应,该金属是_________,写出其中一个反应的化学方程式_________________________________________________________。
(3)性质决定用途,用途反映性质是重要的化学思想。用镁粉制作的烟花在夜空中发出耀眼的白光, 这是利用了镁的________性。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
金属材料在生产和生活中有着广泛的应用.
(1)食品包装袋中经常使用到铝箔,铝能制成铝箔是因为金属具有 性;
(2)铁制品长期暴露在空气中会发生锈蚀,为防止钢铁锈蚀,常采取在其表面涂油漆或镀上其它金属等方法,这些方法能防止锈蚀的共同原理是 .若铁制品已锈蚀,应及时除去铁锈,写出用稀硫酸除去铁锈的化学方程式 ;
(3)将一定质量的铜粉放入硝酸银、硝酸亚铁的混合溶液中,充分反应后过滤,所得滤渣中一定含有的物质是 (填化学式,下同),滤液中一定含有的溶质是 ,反应后所得溶液质量 反应前所得溶液质量(填“>”、“=”或“<”).
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
试回答下列问题:
(1)过程I加入铁屑的主要作用是 ;试写出其对应的化学方程式: ;
(2)从固体中分离出铜需采用的方法是 ;
(3)滤液中溶质主要为 (写出化学式);已知过程II生成的最终产物为Fe(OH)3,则Fe(OH)2与氧气和水反应的化学方程式为: 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
金属在生活和生产中有广泛的应用.
(1)下列金属制品中,利用金属导热性的是 (填字母序号).
(2)铁生锈的条件是 .
(3)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为 .
(4)工业上生产电路板及处理废液的工艺流程如下: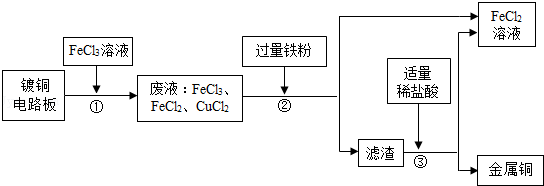
Ⅰ.步骤①反应的化学方程式为 .
Ⅱ.步骤②得到滤渣的成分是 .
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
人们的日常生活离不开金属。请回答下列问题:
(1)奥运场馆“鸟巢”使用了大量的钢铁,钢铁与 直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈。
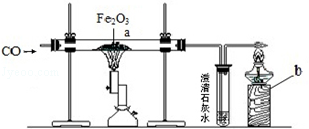
(2)实验室用图示实验模拟炼铁反应的原理。
①a处可观察的现象是 ;
②b处点燃酒精灯的目的是 ;
③为确保实验安全,在通入一氧化碳之前应该 。
(3)置换反应是化学反应的基本类型之一。非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:C12+2NaBr=2NaCl+Br2;I2+Na2S=2NaI+S↓;Br2+2KI=2KBr+I2由此可判断:
①S、C12、I2、Br2活动性由强到弱顺序是 。
②下列化学方程式书写错误的是 。
| A.C12+2NaI=2NaCl+I2 | B.I2+2KBr=2KI+Br2 |
| C.Br2+Na2S=2NaBr+S↓ | D.C12+K2S=2KCl+S↓ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
金属与我们的生活息息相关,在各个领域中用途广泛.
(1)我国第四套人民币硬币从1999年开始发行,一元币为钢芯镀镍(Ni),伍角币为钢芯镀铜合金,一角币为铝合金或不锈钢.选择铸造硬币的材料不需要考虑的因素是 (填序号).
| A.金属的硬度 | B.金属的导电性; |
| C.金属的耐腐蚀性 | D.金属价格与硬币面值的吻合度. |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
在学习金属的性质时,老师拿来了三种外观酷似金、银、铜的样品,同学们对样品进行以下探究:
①用锤子砸“金”,样品粉碎;
②加入稀盐酸:“金”和“铜”没有现象,“银”有大量气泡产生;
③测定密度:“金”4.9g/cm3,“银”7.1g/cm3,“铜”7.5g/cm3.
④查阅几种常见金属的密度,如下表:
| 金属 | 金 | 银 | 铜 | 铁 | 锌 |
| 密度(g/cm3) | 19.3 | 10.5 | 8.9 | 7.9 | 7.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com